Присмасол

Инструкция по применению Присмасол
Перевод выполнен с помощью ИИ
Информация представлена в справочных целях и не заменяет консультацию врача. Перед приемом любых лекарств рекомендуется проконсультироваться с врачом. Oladoctor не несет ответственности за решения, принятые на основе этого материала.
Показать переводСодержание инструкции
- Ulotka dołączona do opakowania: informacja dla użytkownika
- Prismasol 2 mmol/l potasu
- Co to jest Prismasol i w jakim celu się go stosuje
- Informacje ważne przed zastosowaniem leku Prismasol
- Jak stosować Prismasol
- Możliwe działania niepożądane
- Jak przechowywać Prismasol
- Zawartość opakowania i inne informacje
- Co zawiera Prismasol
- Substancje czynne:
- Przed odtworzeniem/zmieszaniem:
- 1000 ml roztworu elektrolitowego (mała komora A) zawiera:
- 1000 ml roztworu buforowego (duża komora B) zawiera:
- Po odtworzeniu/zmieszaniu:
- Jak wygląda Prismasol i co zawiera opakowanie
- Podmiot odpowiedzialny i wytwórca:
- Wytwórca:
- Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
- Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
- Data ostatniej aktualizacji ulotki: wrzesień 2024
- Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
- Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
- Środki ostrożności:
- Sposób podawania:
- Dawkowanie:
- Dzieci i młodzież
- Instrukcja postępowania:
- I
- II
- III
- IV
- Ulotka dołączona do opakowania: informacja dla użytkownika
- Prismasol 2 mmol/l potasu
- Wapnia chlorek dwuwodny/ magnezu chlorek sześciowodny/ glukoza jednowodna/ kwasu mlekowego roztwór 90% w/w/ sodu chlorek/ potasu chlorek/ sodu wodorowęglan
- Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Spis treści ulotki
- Co to jest Prismasol i w jakim celu się go stosuje
- Informacje ważne przed zastosowaniem leku Prismasol
- Jak stosować Prismasol
- Możliwe działania niepożądane
- Jak przechowywać Prismasol
- Zawartość opakowania i inne informacje
- Co zawiera Prismasol
- Substancje czynne:
- Przed odtworzeniem/zmieszaniem:
- 1000 ml roztworu elektrolitowego (mała komora A) zawiera:
- 1000 ml roztworu buforowego (duża komora B) zawiera:
- Po odtworzeniu/zmieszaniu:
- Jak wygląda Prismasol i co zawiera opakowanie
- Podmiot odpowiedzialny i wytwórca:
- Wytwórca:
- Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
- Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
- Data ostatniej aktualizacji ulotki: wrzesień 2024
- Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
- Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
- Środki ostrożności:
- Sposób podawania:
- Dawkowanie:
- Dzieci i młodzież
- Instrukcja postępowania:
- I
- II
- III
- IV
- V
- V.a
- Ulotka dołączona do opakowania: informacja dla użytkownika
- Prismasol 2 mmol/l potasu
- Wapnia chlorek dwuwodny/ magnezu chlorek sześciowodny/ glukoza jednowodna/ kwasu mlekowego roztwór 90% w/w/ sodu chlorek/ potasu chlorek/ sodu wodorowęglan
- Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Spis treści ulotki
- Co to jest Prismasol i w jakim celu się go stosuje
- Informacje ważne przed zastosowaniem leku Prismasol
- Jak stosować Prismasol
- Możliwe działania niepożądane
- Jak przechowywać Prismasol
- Zawartość opakowania i inne informacje
- Co zawiera Prismasol
- Substancje czynne:
- Przed odtworzeniem/zmieszaniem:
- 1000 ml roztworu elektrolitowego (mała komora A) zawiera:
- 1000 ml roztworu buforowego (duża komora B) zawiera:
- Po odtworzeniu/zmieszaniu:
- Jak wygląda Prismasol i co zawiera opakowanie
- Podmiot odpowiedzialny i wytwórca:
- Wytwórca:
- Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
- Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
- Data ostatniej aktualizacji ulotki: wrzesień 2024
- Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
- Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
- Środki ostrożności:
- Sposób podawania:
- Dawkowanie:
- Dzieci i młodzież
- Instrukcja postępowania:
- I
- II
- III
- IV
- V
- V.a
Ulotka dołączona do opakowania: informacja dla użytkownika
Prismasol 2 mmol/l potasu
Roztwór do hemodializy/hemofiltracji
Wapnia chlorek dwuwodny/ magnezu chlorek sześciowodny/ glukoza jednowodna/ kwasu mlekowego roztwór 90% w/w/ sodu chlorek/ potasu chlorek/ sodu wodorowęglan
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Prismasol i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Prismasol
- 3. Jak stosować Prismasol
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Prismasol
- 6. Zawartość opakowania i inne informacje
1. Co to jest Prismasol i w jakim celu się go stosuje
Prismasol zawiera substancje czynne: wapnia chlorek dwuwodny, magnezu chlorek sześciowodny,
glukoza jednowodna, kwasu mlekowego roztwór 90% w/w, sodu chlorek, potasu chlorek, sodu
wodorowęglan.
Prismasol jest stosowany w leczeniu niewydolności nerek jako roztwór do ciągłej hemofiltracji lub
hemodiafiltracji (jako roztwór substytucyjny przy utracie płynów z krwi przepływającej przez filtr)
oraz ciągłej hemodializy lub hemodiafiltracji (krew przepływa po jednej stronie membrany
dializacyjnej, podczas gdy roztwór do hemodializy przepływa po drugiej stronie membrany).
Prismasol można również stosować w przypadku zatrucia lekami zawierającymi substancje ulegające
dializie lub filtracji.
Prismasol 2 mmol/l potasu jest wskazany szczególnie u pacjentów, mających skłonność
do hiperkaliemii (wysokie stężenie potasu we krwi).
2. Informacje ważne przed zastosowaniem leku Prismasol
Nie należy stosować roztworu Prismasol 2 mmol/l potasu w przypadku:
- uczulenia na jedną z substancji czynnych lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- niskiego stężenia potasu we krwi (hipokaliemii),
- wysokiego stężenia wodorowęglanu we krwi (alkalozy metabolicznej).
Nie można wykluczyć obecności antygenu kukurydzy w roztworze Prismasol.
Nie stosować hemofiltracji/dializy w następujących przypadkach:
- niewydolność nerek z wyraźnym hiperkatabolizmem (nieprawidłowy wzrost katabolizmu), jeśli objawów uremii (objawy spowodowane wysokim stężeniem mocznika we krwi) nie można
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
złagodzić za pomocą hemofiltracji;
- niewystarczające ciśnienie tętnicze w dostępie naczyniowym;
- antykoagulacja ogólnoustrojowa (zmniejszona krzepliwość krwi) przy zagrożeniu krwotokiem (krwawieniem).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania roztworu Prismasol należy zwrócić się do lekarza, farmaceuty lub
pielęgniarki.
Roztwór powinien być używany wyłącznie przez lub pod nadzorem lekarza wykwalifikowanego
w leczeniu niewydolności nerek przez zastosowanie hemofiltracji, hemodiafiltracji i ciągłej
hemodializy.
Przed zastosowaniem leczenia i podczas jego trwania zostanie zbadana krew pacjenta, np. będzie
monitorowana równowaga kwasowo-zasadowa i stężenie elektrolitów (soli we krwi), w tym również
wszelkich podawanych płynów (infuzje dożylne) oraz tworzonych przez organizm (wytwarzanie
moczu), nawet niezwiązanych bezpośrednio z terapią.
Należy dokładnie monitorować stężenie glukozy we krwi, zwłaszcza gdy pacjent choruje na cukrzycę.
Lek Prismasol a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio a także o lekach, które pacjent planuje przyjmować.
Stężenie we krwi innych przyjmowanych leków może zostać obniżone podczas leczenia. Lekarz
zdecyduje, czy wymagana jest zmiana przyjmowanych leków.
W szczególności należy powiedzieć lekarzowi o przyjmowaniu następujących leków:
- glikozydów (stosowanych w leczeniu określonych chorób serca), gdyż podczas hipokaliemii (obniżonego stężenia potasu we krwi) zwiększają one ryzyko wystąpienia zaburzeń rytmu serca (nieregularnego lub przyspieszonego bicia serca);
- witaminy D i leków zawierających wapń, gdyż mogą one zwiększać ryzyko wystąpienia hiperkalcemii (wysokiego stężenia wapnia we krwi);
- jakichkolwiek dodatków sodu wodorowęglanu (lub innych buforów), gdyż może on zwiększać ryzyko wystąpienia zasadowicy metabolicznej (nadmiaru wodorowęglanów we krwi);
- cytrynianu, używanego jako środek hamujący krzepnięcie krwi (jako ochronny dodatek w sprzęcie do dializy), ponieważ może on zmniejszyć stężenie wapnia w osoczu.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Lekarz zadecyduje o podawaniu roztworu Prismasol kobietom w ciąży lub karmiącym piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie wiadomo, czy Prismasol wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn.
3. Jak stosować Prismasol
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości
należy zwrócić się do lekarza lub farmaceuty.
Objętość używanego roztworu Prismasol zależy od stanu klinicznego pacjenta i docelowego bilansu
płynów. Dlatego decyzję o objętości dawki podejmuje lekarz odpowiedzialny za leczenie.
Droga podawania: do podawania dożylnego i hemodializy.
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
Zastosowanie większej niż zalecana dawki leku Prismasol
Pacjent będzie miał dokładnie monitorowany bilans płynów, równowagę elektrolitową i kwasowo-
zasadową.
W mało prawdopodobnym przypadku wystąpienia przedawkowania lekarz podejmie niezbędne środki
zaradcze i dostosuje dawkę pacjenta.
Przedawkowanie może prowadzić do wystąpienia:
- przeciążenia płynami we krwi pacjenta,
- wzrostu stężenia wodorowęglanów we krwi (alkaloza metaboliczna)
- i (lub) zmniejszenia stężenia soli we krwi (hipofosfatemia, hipokaliemia). Przedawkowanie może prowadzić do poważnych następstw, takich jak zastoinowa niewydolność serca, zaburzenia równowagi elektrolitowej czy kwasowo-zasadowej.
Instrukcje użycia znajdują się w części „Informacje przeznaczone wyłącznie dla fachowego personelu
medycznego”.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić
się do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Zgłaszano następujące działania niepożądane:
Częstość nieznana: częstość nie może być określona na podstawie dostępnych danych
- zmiany stężenia soli we krwi (zaburzenia równowagi elektrolitowej, jak hipofosfatemia lub hipokaliemia)
- wzrost stężenia wodorowęglanów w osoczu (alkaloza metaboliczna) lub obniżenie stężenia wodorowęglanów w osoczu (kwasica metaboliczna)
- nieprawidłowo wysoka lub niska objętość wody w organizmie (hiper- lub hipowolemia)
- nieprawidłowo wysokie stężenie glukozy we krwi (hiperglikemia)
- nudności
- wymioty
- skurcze mięśni
- niedociśnienie (niskie ciśnienie krwi).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania
niepożądane
można
zgłaszać
bezpośrednio
do
Departamentu
Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
5. Jak przechowywać Prismasol
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze poniżej +4°C.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i opakowaniu. Termin
ważności oznacza ostatni dzień podanego miesiąca.
Wykazano chemiczną i fizyczną stabilność gotowego do użycia roztworu w ciągu 24 godzin w
temperaturze +22°C. Jeśli nie zostanie zużyty od razu, za czas i warunki przechowywania przed
zastosowaniem odpowiada użytkownik i czas ten nie powinien być dłuższy niż 24 godziny, włączając
czas leczenia.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Prismasol
Substancje czynne:
Przed odtworzeniem/zmieszaniem:
1000 ml roztworu elektrolitowego (mała komora A) zawiera:
Wapnia chlorek dwuwodny
5,145 g
Magnezu chlorek sześciowodny
2,033 g
Glukoza
22,000 g
Kwas (S)-mlekowy
5,400 g
1000 ml roztworu buforowego (duża komora B) zawiera:
Sodu chlorek
6,450 g
Sodu wodorowęglan
3,090 g
Potasu chlorek
0,157 g
Po odtworzeniu/zmieszaniu:
Roztwory w komorach A (250 ml) i B (4750 ml) są mieszane w celu otrzymania jednego gotowego do
użycia roztworu (5000 ml) składającego się z:
mmol/l
mEq/l
Wapń
Ca
1,75
3,50
Magnez
Mg
0,50
1,00
Sód
Na
140,00
140,00
Chlorki
Cl
111,50
111,50
Mleczan
3,00
3,00
Wodorowęglan
HCO
32,00
32,00
Potas
K
2,00
2,00
Glukoza
6,10
Teoretyczna osmolarność:
297 mOsm/l
Pozostałe składniki leku to:dwutlenek węgla (E 290), woda do wstrzykiwań.
pH gotowego do użycia roztworu wynosi: 7,0 do 8,5
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
Jak wygląda Prismasol i co zawiera opakowanie
Prismasol jest pakowany w dwukomorowe worki zawierające w mniejszej komorze A roztwór
elektrolitowy, a w większej komorze B – roztwór buforowy. Ostateczny gotowy do użycia roztwór
uzyskuje się po rozerwaniu rozrywalnego spawu i wymieszaniu obu roztworów. Gotowy do użycia
roztwór jest przezroczysty i lekko żółty. Każdy worek (A+B) zawiera 5000 ml roztworu do
hemofiltracji i hemodializy. Worek jest umieszczony w przezroczystym opakowaniu zewnętrznym.
W każdym opakowaniu znajdują się dwa worki i ulotka informacyjna.
Podmiot odpowiedzialny i wytwórca:
Vantive Belgium SRL
Boulevard d’Angleterre 2
1420 Braine-l’Alleud
Belgia
Wytwórca:
Bieffe Medital S.p.A.,
Via Stelvio 94,
23035 Sondalo (SO),
Włochy
lub
Vantive Manufacturing Limited,
Moneen Road,
Castlebar
County Mayo
F23 XR63
Irlandia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
Austria, Belgia, Bułgaria, Cypr, Czechy, Dania, Estonia, Finlandia, Francja, Niemcy, Grecja, Węgry,
Islandia, Irlandia, Włochy, Łotwa, Litwa, Luksemburg, Malta, Holandia, Norwegia, Polska,
Portugalia, Rumunia, Słowacja, Słowenia, Hiszpania, Szwecja, Wielka Brytania (Irlandia Północna):
Prismasol 2.
Data ostatniej aktualizacji ulotki: wrzesień 2024
--------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
Środki ostrożności:
Należy ściśle przestrzegać instrukcji użycia/postępowania z produktem leczniczym Prismasol.
Roztwory z obu komór muszązostać zmieszane przed użyciem.
Zastosowanie zanieczyszczonego roztworu do hemofiltracji oraz hemodializy może spowodować
sepsę, wstrząs lub stan zagrażający życiu.
Aby zwiększyć komfort pacjenta, produkt leczniczy Prismasol można ogrzać do temperatury 37°C.
Ogrzanie roztworu przed użyciem należy wykonać przed rekonstytucją i wyłącznie przy użyciu
suchego źródła ciepła. Roztworów nie należy ogrzewać w wodzie ani kuchence mikrofalowej. Przed
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
podaniem należy sprawdzić wizualnie roztwór w celu wykrycia obecności cząstek stałych oraz zmiany
zabarwienia, o ile roztwór oraz opakowanie na to pozwalają. Nie podawać roztworu, który nie jest
przezroczysty lub spaw został naruszony.
Roztwór ten zawiera potas. Stężenie potasu w surowicy musi być monitorowane przed zabiegiem
hemofiltracji i (lub) hemodializy oraz podczas jego trwania. Zależnie od stężenia potasu w surowicy
przed leczeniem może rozwinąć się hipokaliemia lub hiperkaliemia.
Jeśli wystąpi hipokaliemia, może być koniecznie dodanie potasu i (lub) podanie dializatu o wyższym
stężeniu potasu.
Jeśli po rozpoczęciu leczenia wystąpi hiperkaliemia, należy ocenić dodatkowe źródła wpływające na
stężenie potasu we krwi. Jeśli roztwór stosuje się jako roztwór substytucyjny, należy zmniejszyć
szybkość infuzji i potwierdzić, że osiągnięto żądane stężenie potasu. Jeśli hiperkaliemia nie ustąpi,
należy natychmiast przerwać infuzję.
Jeśli hiperkaliemia rozwinie się w przypadku stosowania roztworu jako dializatu, może być konieczne
podanie dializatu niezawierającego potasu w celu zwiększenia szybkości usuwania potasu.
Należy regularnie mierzyć stężenie nieorganicznych fosforanów. W przypadku niskiego stężenia
fosforanów we krwi, nieorganiczne fosforany muszą być uzupełniane. Do roztworu można dodać
fosforany w ilości do 1,2 mmol/l. W przypadku dodawania potasu fosforanu całkowite stężenie potasu
nie powinno przekraczać 4 mEq/l (4 mmol/l).
Choć w związku ze stosowaniem produktu leczniczego Prismasol nie zgłaszano przypadków ciężkich
reakcji nadwrażliwości na kukurydzę, roztwory zawierające glukozę uzyskaną z hydrolizowanej
skrobi kukurydzianej nie powinny być stosowane u pacjentów ze stwierdzoną alergią na kukurydzę
lub produkty kukurydziane.
Należy natychmiast przerwać podawanie w przypadku wystąpienia jakichkolwiek przedmiotowych
lub podmiotowych objawów podejrzewanej reakcji nadwrażliwości. Należy zastosować odpowiednie
terapeutyczne środki zaradcze zgodnie ze wskazaniem klinicznym.
Ponieważ roztwór zawiera glukozę oraz mleczan, może się rozwinąć hiperglikemia, zwłaszcza
u pacjentów chorych na cukrzycę. Należy regularnie monitorować stężenie glukozy we krwi. Jeśli
rozwinie się hiperglikemia, może być konieczne podanie roztworu substytucyjnego/dializatu
niezawierającego glukozy. Mogą być konieczne inne środki zaradcze w celu utrzymania pożądanej
wartości glikemii.
Produkt leczniczy Prismasol zawiera wodorowęglan (dwuwęglan) oraz mleczan (prekursor
wodorowęglanu), które mogą wpływać na równowagę kwasowo-zasadową pacjenta. Jeśli w trakcie
leczenia z użyciem roztworu wystąpi lub pogłębi się alkaloza metaboliczna, może zaistnieć potrzeba
zmniejszenia szybkości podawania lub wstrzymania podawania produktu leczniczego.
Przed rozpoczęciem leczenia oraz podczas jego trwania, należy ściśle monitorować stężenie
elektrolitów oraz równowagę kwasowo-zasadową.
W przypadku braku równowagi płynów należy uważnie monitorować stan kliniczny pacjenta i w razie
potrzeby korygować bilans płynów.
Sposób podawania:
Do podawania dożylnego i hemodializy. Prismasol używany jako roztwór substytucyjny jest
podawany do obwodu przed hemofiltrem (predylucja) lub za hemofiltrem (postdylucja).
Dawkowanie:
Objętość oraz szybkość podawania używanego roztworu Prismasol zależy od stężenia elektrolitów we
krwi, równowagi kwasowo-zasadowej oraz ogólnego stanu klinicznego pacjenta. Parametry
podawania (dawkę, szybkość infuzji, całkowitą objętość) produktu Prismasol powinien ustalać lekarz.
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
Szybkości przepływu dla roztworu substytucyjnego w hemofiltracji i hemodiafiltracji wynoszą:
Dorośli:
500 do 3000 ml/godz.
Szybkości przepływu dla roztworu do dializy (dializat) w ciągłej hemodializie i ciągłej
hemodiafiltracji wynoszą:
Dorośli:
500 do 2500 ml/godz.
Najczęściej stosowane szybkości przepływu w przypadku dorosłych wynoszą około 2000 do
2500 ml/godz., co odpowiada dobowej objętości płynu wynoszącej około 48 do 60 l.
Dzieci i młodzież
Zakres szybkości przepływu roztworu substytucyjnego w hemofiltracji i hemodiafiltracji oraz
roztworu do dializy (dializatu) w ciągłej hemodializie wynosi:
dzieci (od noworodków po młodzież do 18 lat): 1000 do 2000 ml/godz./1,73 m .
Wymagane szybkości przepływu mogą wynosić do 4000 ml/godz./1,73 m , zwłaszcza u młodszych
dzieci (≤10 kg). Bezwzględna szybkość przepływu (w ml/godz.) u dzieci i młodzieży zazwyczaj nie
powinna przekraczać maksymalnej szybkości przepływu stosowanej u dorosłych.
Instrukcja postępowania:
Aby uzyskać gotowy do użycia roztwór, roztwór elektrolitowy (mała komora A) jest dodawany do
roztworu buforowego (duża komora B) poprzez otwarcie rozrywalnego spawu bezpośrednio przed
użyciem.
Należy stosować wyłącznie z odpowiednim sprzętem do pozaustrojowej wymiany nerkowej.
Podczas postępowania i podawania produktu pacjentowi należy stosować technikę aseptyczną.
Użyć wyłącznie, gdy opakowanie ochronne nie jest uszkodzone, wszystkie spawy są nienaruszone,
rozrywalny spaw nie jest uszkodzony, a roztwór jest przezroczysty. Ścisnąć mocno worek, aby
sprawdzić jego szczelność. W przypadku stwierdzenia przecieku roztwór należy natychmiast
wyrzucić, ponieważ nie można już zapewnić jego jałowości.
Duża komora B wyposażona jest w port do wstrzykiwań, umożliwiający po rekonstytucji roztworu,
dodanie innych niezbędnych produktów leczniczych. Lekarz jest odpowiedzialny za określenie
zgodności dodatkowych produktów leczniczych z roztworem Prismasol poprzez sprawdzanie czy nie
nastąpiła zmiana koloru i (lub) wytrącenie się osadu, nierozpuszczalnych kompleksów lub kryształów.
Przed dodaniem produktu leczniczego należy sprawdzić, czy jest rozpuszczalny i stabilny w wodzie o
pH takim jak roztwór Prismasol (pH gotowego do użycia roztworu wynosi od 7,0 do 8,5). Dodatkowe
składniki mogą być niezgodne. Należy zapoznać się z instrukcją dotyczącą stosowania dodawanego
produktu leczniczego.
Usunąć płyn z portu do wstrzykiwań, przytrzymać worek do góry nogami, wstrzyknąć produkt
leczniczy przez port i starannie wymieszać. Roztwór należy podać niezwłocznie. Dodatkowe składniki
muszą zawsze być dodane i zmieszane przed podłączeniem worka z roztworem do obwodu
pozaustrojowego.
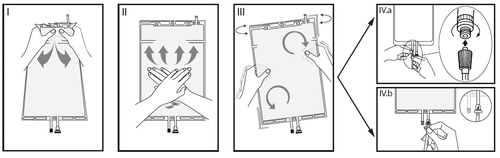
I
Opakowanie zewnętrzne zdjąć bezpośrednio przed użyciem i wymieszać roztwory z dwóch
różnych komór. Trzymając małą komorę oburącz i ściskając do momentu powstania otworu w
rozrywalnym spawie oddzielającym obydwie komory. (Patrz rysunek I poniżej)
II
Nacisnąć dużą komorę oburącz do momentu całkowitego otwarcia rozrywalnego spawu
pomiędzy dwiema komorami. (Patrz rysunek II poniżej)
III
Zapewnić dokładne wymieszanie poprzez delikatne wstrząsanie workiem. Roztwór jest teraz
gotowy do użycia, a worek można powiesić na stojaku. (Patrz rysunek III poniżej)
IV
Do każdego z dwóch portów dostępu można podłączyć linię dializy lub wymiany.
IV.aJeśli korzysta się z dostępu typu luer, usunąć zatyczkę, przekręcając ją i pociągając, a następnie
podłączyć męską końcówkę luer lock linii dializy lub wymiany do żeńskiej końcówki typu luer
receptor na worku, dociskając ją i przekręcając. Upewnić się, że połączenie jest całkowicie
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
osadzone i pewne. Teraz złącze jest otwarte. Sprawdzić, czy płyn przepływa swobodnie. (Patrz
rysunek IV.a poniżej)
Gdy linie dializy lub wymiany są odłączone od złącza typu luer, połączenie zostanie zamknięte i
przepływ płynu wstrzymany. Port typu luer jest bezigłowy i można go przecierać środkami
dezynfekującymi.
IV.bJeśli używany jest port do wstrzykiwań, najpierw usunąć zatyczkę poprzez jej odłamanie. Port
do wstrzykiwań można przecierać środkami dezynfekującymi. Następnie przebić kolcem
gumową przegrodę. Sprawdzić, czy płyn przepływa swobodnie. (Patrz rysunek IV.b poniżej)
Roztwór należy użyć niezwłocznie po usunięciu zewnętrznego opakowania. Jeśli nie zostanie użyty od
razu, odtworzony roztwór należy użyć w ciągu 24 godzin, włączając w to czas zabiegu po dodaniu
roztworu elektrolitowego oraz roztworu buforowego.
Gotowy do użycia roztwór przeznaczony jest wyłącznie do jednorazowego użytku. Wyrzucić cały
niezużyty roztwór bezpośrednio po użyciu.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
Prismasol 2 mmol/l Potassium / PL / PL Polyolefin luer connector with valve
Ulotka dołączona do opakowania: informacja dla użytkownika
Prismasol 2 mmol/l potasu
Roztwór do hemodializy/hemofiltracji
Wapnia chlorek dwuwodny/ magnezu chlorek sześciowodny/ glukoza jednowodna/ kwasu mlekowego roztwór 90% w/w/ sodu chlorek/ potasu chlorek/ sodu wodorowęglan
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Prismasol i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Prismasol
- 3. Jak stosować Prismasol
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Prismasol
- 6. Zawartość opakowania i inne informacje
1. Co to jest Prismasol i w jakim celu się go stosuje
Prismasol zawiera substancje czynne: wapnia chlorek dwuwodny, magnezu chlorek sześciowodny,
glukoza jednowodna, kwasu mlekowego roztwór 90% w/w, sodu chlorek, potasu chlorek, sodu
wodorowęglan.
Prismasol jest stosowany w leczeniu niewydolności nerek jako roztwór do ciągłej hemofiltracji lub
hemodiafiltracji (jako roztwór substytucyjny przy utracie płynów z krwi przepływającej przez filtr)
oraz ciągłej hemodializy lub hemodiafiltracji (krew przepływa po jednej stronie membrany
dializacyjnej, podczas gdy roztwór do hemodializy przepływa po drugiej stronie membrany).
Prismasol można również stosować w przypadku zatrucia lekami zawierającymi substancje ulegające
dializie lub filtracji.
Prismasol 2 mmol/l potasu jest wskazany szczególnie u pacjentów, mających skłonność
do hiperkaliemii (wysokie stężenie potasu we krwi).
2. Informacje ważne przed zastosowaniem leku Prismasol
Nie należy stosować roztworu Prismasol 2 mmol/l potasu w przypadku:
- uczulenia na jedną z substancji czynnych lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- niskiego stężenia potasu we krwi (hipokaliemii),
- wysokiego stężenia wodorowęglanu we krwi (alkalozy metabolicznej).
Nie można wykluczyć obecności antygenu kukurydzy w roztworze Prismasol.
Nie stosować hemofiltracji/dializy w następujących przypadkach:
- niewydolność nerek z wyraźnym hiperkatabolizmem (nieprawidłowy wzrost katabolizmu), jeśli objawów uremii (objawy spowodowane wysokim stężeniem mocznika we krwi) nie można
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
1/8
złagodzić za pomocą hemofiltracji;
- niewystarczające ciśnienie tętnicze w dostępie naczyniowym;
- antykoagulacja ogólnoustrojowa (zmniejszona krzepliwość krwi) przy zagrożeniu krwotokiem (krwawieniem).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania roztworu Prismasol należy zwrócić się do lekarza, farmaceuty lub
pielęgniarki.
Roztwór powinien być używany wyłącznie przez lub pod nadzorem lekarza wykwalifikowanego
w leczeniu niewydolności nerek przez zastosowanie hemofiltracji, hemodiafiltracji i ciągłej
hemodializy.
Przed zastosowaniem leczenia i podczas jego trwania zostanie zbadana krew pacjenta, np. będzie
monitorowana równowaga kwasowo-zasadowa i stężenie elektrolitów (soli we krwi), w tym również
wszelkich podawanych płynów (infuzje dożylne) oraz tworzonych przez organizm (wytwarzanie
moczu), nawet niezwiązanych bezpośrednio z terapią.
Należy dokładnie monitorować stężenie glukozy we krwi, zwłaszcza gdy pacjent choruje na cukrzycę.
Lek Prismasol a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio a także o lekach, które pacjent planuje przyjmować.
Stężenie we krwi innych przyjmowanych leków może zostać obniżone podczas leczenia. Lekarz
zdecyduje, czy wymagana jest zmiana przyjmowanych leków.
W szczególności należy powiedzieć lekarzowi o przyjmowaniu następujących leków:
- glikozydów (stosowanych w leczeniu określonych chorób serca), gdyż podczas hipokaliemii (obniżonego stężenia potasu we krwi) zwiększają one ryzyko wystąpienia zaburzeń rytmu serca (nieregularnego lub przyspieszonego bicia serca);
- witaminy D i leków zawierających wapń, gdyż mogą one zwiększać ryzyko wystąpienia hiperkalcemii (wysokiego stężenia wapnia we krwi);
- jakichkolwiek dodatków sodu wodorowęglanu (lub innych buforów), gdyż może on zwiększać ryzyko wystąpienia zasadowicy metabolicznej (nadmiaru wodorowęglanów we krwi);
- cytrynianu, używanego jako środek hamujący krzepnięcie krwi (jako ochronny dodatek w sprzęcie do dializy), ponieważ może on zmniejszyć stężenie wapnia w osoczu.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Lekarz zadecyduje o podawaniu roztworu Prismasol kobietom w ciąży lub karmiącym piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie wiadomo, czy Prismasol wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn.
3. Jak stosować Prismasol
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości
należy zwrócić się do lekarza lub farmaceuty.
Objętość używanego roztworu Prismasol zależy od stanu klinicznego pacjenta i docelowego bilansu
płynów. Dlatego decyzję o objętości dawki podejmuje lekarz odpowiedzialny za leczenie.
Droga podawania: do podawania dożylnego i hemodializy.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
2/8
Zastosowanie większej niż zalecana dawki leku Prismasol
Pacjent będzie miał dokładnie monitorowany bilans płynów, równowagę elektrolitową i kwasowo-
zasadową.
W mało prawdopodobnym przypadku wystąpienia przedawkowania lekarz podejmie niezbędne środki
zaradcze i dostosuje dawkę pacjenta.
Przedawkowanie może prowadzić do wystąpienia:
- przeciążenia płynami we krwi pacjenta,
- wzrostu stężenia wodorowęglanów we krwi (alkaloza metaboliczna)
- i (lub) zmniejszenia stężenia soli we krwi (hipofosfatemia, hipokaliemia). Przedawkowanie może prowadzić do poważnych następstw, takich jak zastoinowa niewydolność serca, zaburzenia równowagi elektrolitowej czy kwasowo-zasadowej.
Instrukcje użycia znajdują się w części „Informacje przeznaczone wyłącznie dla fachowego personelu
medycznego”.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku należy zwrócić się
do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Zgłaszano następujące działania niepożądane:
Częstość nieznana: częstość nie może być określona na podstawie dostępnych danych
- zmiany stężenia soli we krwi (zaburzenia równowagi elektrolitowej, jak hipofosfatemia lub hipokaliemia)
- wzrost stężenia wodorowęglanów w osoczu (alkaloza metaboliczna) lub obniżenie stężenia wodorowęglanów w osoczu (kwasica metaboliczna)
- nieprawidłowo wysoka lub niska objętość wody w organizmie (hiper- lub hipowolemia)
- nieprawidłowo wysokie stężenie glukozy we krwi (hiperglikemia)
- nudności
- wymioty
- skurcze mięśni
- niedociśnienie (niskie ciśnienie krwi).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania
niepożądane
można
zgłaszać
bezpośrednio
do
Departamentu
Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
3/8
5. Jak przechowywać Prismasol
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze poniżej +4°C.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i opakowaniu. Termin
ważności oznacza ostatni dzień podanego miesiąca.
Wykazano chemiczną i fizyczną stabilność gotowego do użycia roztworu w ciągu 24 godzin w
temperaturze +22°C. Jeśli nie zostanie zużyty od razu, za czas i warunki przechowywania przed
zastosowaniem odpowiada użytkownik i czas ten nie powinien być dłuższy niż 24 godziny, włączając
czas leczenia.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Prismasol
Substancje czynne:
Przed odtworzeniem/zmieszaniem:
1000 ml roztworu elektrolitowego (mała komora A) zawiera:
Wapnia chlorek dwuwodny
5,145 g
Magnezu chlorek sześciowodny
2,033 g
Glukoza
22,000 g
Kwas (S)-mlekowy
5,400 g
1000 ml roztworu buforowego (duża komora B) zawiera:
Sodu chlorek
6,450 g
Sodu wodorowęglan
3,090 g
Potasu chlorek
0,157 g
Po odtworzeniu/zmieszaniu:
Roztwory w komorach A (250 ml) i B (4750 ml) są mieszane w celu otrzymania jednego gotowego do
użycia roztworu (5000 ml) składającego się z:
mmol/l
mEq/l
Wapń
Ca
1,75
3,50
Magnez
Mg
0,50
1,00
Sód
Na
140,00
140,00
Chlorki
Cl
111,50
111,50
Mleczan
3,00
3,00
Wodorowęglan
HCO
32,00
32,00
Potas
K
2,00
2,00
Glukoza
6,10
Teoretyczna osmolarność:
297 mOsm/l
Pozostałe składniki leku to:dwutlenek węgla (E 290), woda do wstrzykiwań.
pH gotowego do użycia roztworu wynosi: 7,0 do 8,5
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
4/8
Jak wygląda Prismasol i co zawiera opakowanie
Prismasol jest pakowany w dwukomorowe worki zawierające w mniejszej komorze A roztwór
elektrolitowy, a w większej komorze B – roztwór buforowy. Ostateczny gotowy do użycia roztwór
uzyskuje się po złamaniu łamliwej zatyczki i wymieszaniu obu roztworów. Gotowy do użycia roztwór
jest przezroczysty i lekko żółty. Każdy worek (A+B) zawiera 5000 ml roztworu do hemofiltracji
i hemodializy. Worek jest umieszczony w przezroczystym opakowaniu zewnętrznym.
W każdym opakowaniu znajdują się dwa worki i ulotka informacyjna.
Podmiot odpowiedzialny i wytwórca:
Vantive Belgium SRL
Boulevard d’Angleterre 2
1420 Braine-l’Alleud
Belgia
Wytwórca:
Bieffe Medital S.p.A.,
Via Stelvio 94,
23035 Sondalo (SO),
Włochy
lub
Vantive Manufacturing Limited,
Moneen Road,
Castlebar
County Mayo
F23 XR63
Irlandia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
Austria, Belgia, Bułgaria, Cypr, Czechy, Dania, Estonia, Finlandia, Francja, Niemcy, Grecja, Węgry,
Islandia, Irlandia, Włochy, Łotwa, Litwa, Luksemburg, Malta, Holandia, Norwegia, Polska,
Portugalia, Rumunia, Słowacja, Słowenia, Hiszpania, Szwecja, Wielka Brytania (Irlandia Północna):
Prismasol 2.
Data ostatniej aktualizacji ulotki: wrzesień 2024
--------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
Środki ostrożności:
Należy ściśle przestrzegać instrukcji użycia/postępowania z produktem leczniczym Prismasol.
Roztwory z obu komór muszą zostać zmieszaneprzed użyciem.
Zastosowanie zanieczyszczonego roztworu do hemofiltracji oraz hemodializy może spowodować
sepsę, wstrząs lub stan zagrażający życiu.
Aby zwiększyć komfort pacjenta, produkt leczniczy Prismasol można ogrzać do temperatury 37°C.
Ogrzanie roztworu przed użyciem należy wykonać przed rekonstytucją i wyłącznie przy użyciu
suchego źródła ciepła. Roztworów nie należy ogrzewać w wodzie ani kuchence mikrofalowej. Przed
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
5/8
podaniem należy sprawdzić wizualnie roztwór w celu wykrycia obecności cząstek stałych oraz zmiany
zabarwienia, o ile roztwór oraz opakowanie na to pozwalają. Nie podawać roztworu, który nie jest
przezroczysty lub spaw został naruszony.
Roztwór ten zawiera potas. Stężenie potasu w surowicy musi być monitorowane przed zabiegiem
hemofiltracji i (lub) hemodializy oraz podczas jego trwania. Zależnie od stężenia potasu w surowicy
przed leczeniem może rozwinąć się hipokaliemia lub hiperkaliemia.
Jeśli wystąpi hipokaliemia, może być koniecznie dodanie potasu i (lub) podanie dializatu o wyższym
stężeniu potasu.
Jeśli po rozpoczęciu leczenia wystąpi hiperkaliemia, należy ocenić dodatkowe źródła wpływające na
stężenie potasu we krwi. Jeśli roztwór stosuje się jako roztwór substytucyjny, należy zmniejszyć
szybkość infuzji i potwierdzić, że osiągnięto żądane stężenie potasu. Jeśli hiperkaliemia nie ustąpi,
należy natychmiast przerwać infuzję.
Jeśli hiperkaliemia rozwinie się w przypadku stosowania roztworu jako dializatu, może być konieczne
podanie dializatu niezawierającego potasu w celu zwiększenia szybkości usuwania potasu.
Należy regularnie mierzyć stężenie nieorganicznych fosforanów. W przypadku niskiego stężenia
fosforanów we krwi, nieorganiczne fosforany muszą być uzupełniane. Do roztworu można dodać
fosforany w ilości do 1,2 mmol/l. W przypadku dodawania potasu fosforanu całkowite stężenie potasu
nie powinno przekraczać 4 mEq/l (4 mmol/l).
Choć w związku ze stosowaniem produktu leczniczego Prismasol nie zgłaszano przypadków ciężkich
reakcji nadwrażliwości na kukurydzę, roztwory zawierające glukozę uzyskaną z hydrolizowanej
skrobi kukurydzianej nie powinny być stosowane u pacjentów ze stwierdzoną alergią na kukurydzę
lub produkty kukurydziane.
Należy natychmiast przerwać podawanie w przypadku wystąpienia jakichkolwiek przedmiotowych
lub podmiotowych objawów podejrzewanej reakcji nadwrażliwości. Należy zastosować odpowiednie
terapeutyczne środki zaradcze, zgodnie ze wskazaniem klinicznym.
Ponieważ roztwór zawiera glukozę oraz mleczan, może się rozwinąć hiperglikemia, zwłaszcza
u pacjentów chorych na cukrzycę. Należy regularnie monitorować stężenie glukozy we krwi. Jeśli
rozwinie się hiperglikemia, może być konieczne podanie roztworu substytucyjnego/dializatu
niezawierającego glukozy. Mogą być konieczne inne środki zaradcze w celu utrzymania pożądanej
wartości glikemii.
Produkt leczniczy Prismasol zawiera wodorowęglan (dwuwęglan) oraz mleczan (prekursor
wodorowęglanu), które mogą wpływać na równowagę kwasowo-zasadową pacjenta. Jeśli w trakcie
leczenia z użyciem roztworu wystąpi lub pogłębi się alkaloza metaboliczna, może zaistnieć potrzeba
zmniejszenia szybkości podawania lub wstrzymania podawania produktu leczniczego.
Przed rozpoczęciem leczenia oraz podczas jego trwania, należy ściśle monitorować stężenie
elektrolitów oraz równowagę kwasowo-zasadową.
W przypadku braku równowagi płynów należy uważnie monitorować stan kliniczny pacjenta i w razie
potrzeby korygować bilans płynów.
Sposób podawania:
Do podawania dożylnego i hemodializy. Prismasol używany jako roztwór substytucyjny jest
podawany do obwodu przed hemofiltrem (predylucja) lub za hemofiltrem (postdylucja).
Dawkowanie:
Objętość oraz szybkość podawania używanego roztworu Prismasol zależy od stężenia elektrolitów we
krwi, równowagi kwasowo-zasadowej oraz ogólnego stanu klinicznego pacjenta. Parametry
podawania (dawkę, szybkość infuzji, całkowitą objętość) produktu Prismasol powinien ustalać lekarz.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
6/8
Szybkości przepływu dla roztworu substytucyjnego w hemofiltracji i hemodiafiltracji wynoszą:
Dorośli:
500 do 3000 ml/godz.
Szybkości przepływu dla roztworu do dializy (dializat) w ciągłej hemodializie i ciągłej
hemodiafiltracji wynoszą:
Dorośli:
500 do 2500 ml/godz.
Najczęściej stosowane szybkości przepływu w przypadku dorosłych wynoszą około 2000 do
2500 ml/godz., co odpowiada dobowej objętości płynu wynoszącej około 48 do 60 l.
Dzieci i młodzież
Zakres szybkości przepływu roztworu substytucyjnego w hemofiltracji i hemodiafiltracji oraz
roztworu do dializy (dializatu) w ciągłej hemodializie wynosi:
dzieci (od noworodków po młodzież do 18 lat): 1000 do 2000 ml/godz./1,73 m .
Wymagane szybkości przepływu mogą wynosić do 4000 ml/godz./1,73 m , zwłaszcza u młodszych
dzieci (≤10 kg). Bezwzględna szybkość przepływu (w ml/godz.) u dzieci i młodzieży zazwyczaj nie
powinna przekraczać maksymalnej szybkości przepływu stosowanej u dorosłych.
Instrukcja postępowania:
Aby uzyskać gotowy do użycia roztwór, roztwór elektrolitowy (mała komora A) jest dodawany do
roztworu buforowego (duża komora B) poprzez złamanie łamliwej zatyczki bezpośrednio przed
użyciem.
Należy stosować wyłącznie z odpowiednim sprzętem do pozaustrojowej wymiany nerkowej.
Podczas postępowania i podawania produktu pacjentowi należy stosować technikę aseptyczną.
Użyć wyłącznie, gdy opakowanie ochronne nie jest uszkodzone, wszystkie spawy są nienaruszone,
łamliwa zatyczka nie jest złamana, a roztwór jest przezroczysty. Ścisnąć mocno worek, aby sprawdzić
jego szczelność. W przypadku stwierdzenia przecieku roztwór należy natychmiast wyrzucić, ponieważ
nie można już zapewnić jego jałowości.
Duża komora B wyposażona jest w port do wstrzykiwań, umożliwiający po rekonstytucji roztworu,
dodanie innych niezbędnych produktów leczniczych. Lekarz jest odpowiedzialny za określenie
zgodności dodatkowych produktów leczniczych z roztworem Prismasol poprzez sprawdzanie czy nie
nastąpiła zmiana koloru i (lub) wytrącenie się osadu, nierozpuszczalnych kompleksów lub kryształów.
Przed dodaniem produktu leczniczego należy sprawdzić, czy jest rozpuszczalny i stabilny w wodzie o
pH takim jak roztwór Prismasol (pH gotowego do użycia roztworu wynosi od 7,0 do 8,5). Dodatkowe
składniki mogą być niezgodne. Należy zapoznać się z instrukcją dotyczącą stosowania dodawanego
produktu leczniczego.
Usunąć płyn z portu do wstrzykiwań, przytrzymać worek do góry nogami, wstrzyknąć produkt
leczniczy przez port i starannie wymieszać. Roztwór należy podać niezwłocznie .Dodatkowe składniki
muszą zawsze być dodane i zmieszane przed podłączeniem worka z roztworem do obwodu
pozaustrojowego.
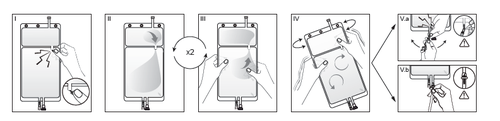
I
Opakowanie zewnętrzne zdjąć bezpośrednio przed użyciem i wyrzucić wszystkie pozostałe
materiały opakowaniowe. Otworzyć zamknięcie łamiąc łamliwą zatyczkę znajdującą się
pomiędzy dwiema komorami worka. Łamliwa zatyczka pozostanie w worku. (Patrz rysunek I
poniżej)
II
Upewnić się, że cały płyn z małej komory A został przelany do dużej komory B. (Patrz rysunek
II poniżej)
III
Przepłukać dwukrotniemałą komorę A, wyciskając zmieszany roztwór z powrotem do małej
komory A, a następnie ponownie do dużej komory B. (Patrz rysunek III poniżej)
IV
Gdy mała komora A jest pusta: potrząsać dużą komorą B w celu całkowitego wymieszania się
jej zawartości. Roztwór jest teraz gotowy do użycia i worek można zawiesić na stojaku. (Patrz
rysunek IV poniżej)
V
Do każdego z dwóch portów dostępu można podłączyć linię dializy lub wymiany.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
7/8
V.a
Jeśli korzysta się z dostępu typu luer, usunąć zatyczkę i podłączyć męską końcówkę luer lock linii
dializy lub wymiany do żeńskiej końcówki typu luer receptor na worku: zacisnąć. Chwytając
kciukiem i palcami złamać niebieską łamliwą zatyczkę u podstawy i poruszać nią tam i z
powrotem. Nie należy używać narzędzia. Należy upewnić się, że zatyczka oddzieliła się
całkowicie i że płyn może przepływać swobodnie. Zatyczka podczas terapii pozostanie w porcie
luer. (Patrz rysunek V.a poniżej)
V.bJeśli używany jest port do wstrzykiwań, najpierw usunąć zatyczkę poprzez jej odłamanie. Port
do wstrzykiwań można przecierać środkami dezynfekującymi. Następnie przebić kolcem
gumową przegrodę. Sprawdzić, czy płyn przepływa swobodnie. (Patrz rysunek V.b poniżej)
Roztwór należy użyć niezwłocznie po usunięciu zewnętrznego opakowania. Jeśli nie zostanie użyty od
razu, odtworzony roztwór należy użyć w ciągu 24 godzin, włączając w to czas zabiegu po dodaniu
roztworu elektrolitowego oraz roztworu buforowego.
Gotowy do użycia roztwór przeznaczony jest wyłącznie do jednorazowego użytku. Wyrzucić cały
niezużyty roztwór bezpośrednio po użyciu.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with pin
8/8
Ulotka dołączona do opakowania: informacja dla użytkownika
Prismasol 2 mmol/l potasu
Roztwór do hemodializy/hemofiltracji
Wapnia chlorek dwuwodny/ magnezu chlorek sześciowodny/ glukoza jednowodna/ kwasu mlekowego roztwór 90% w/w/ sodu chlorek/ potasu chlorek/ sodu wodorowęglan
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza, farmaceuty lub pielęgniarki.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest Prismasol i w jakim celu się go stosuje
- 2. Informacje ważne przed zastosowaniem leku Prismasol
- 3. Jak stosować Prismasol
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać Prismasol
- 6. Zawartość opakowania i inne informacje
1. Co to jest Prismasol i w jakim celu się go stosuje
Prismasol zawiera substancje czynne: wapnia chlorek dwuwodny, magnezu chlorek sześciowodny,
glukoza jednowodna, kwasu mlekowego roztwór 90% w/w, sodu chlorek, potasu chlorek, sodu
wodorowęglan.
Prismasol jest stosowany w leczeniu niewydolności nerek jako roztwór do ciągłej hemofiltracji lub
hemodiafiltracji (jako roztwór substytucyjny przy utracie płynów z krwi przepływającej przez filtr)
oraz ciągłej hemodializy lub hemodiafiltracji (krew przepływa po jednej stronie membrany
dializacyjnej, podczas gdy roztwór do hemodializy przepływa po drugiej stronie membrany).
Prismasol można również stosować w przypadku zatrucia lekami zawierającymi substancje ulegające
dializie lub filtracji.
Prismasol 2 mmol/l potasu jest wskazany szczególnie u pacjentów, mających skłonność
do hiperkaliemii (wysokie stężenie potasu we krwi).
2. Informacje ważne przed zastosowaniem leku Prismasol
Nie należy stosować roztworu Prismasol 2 mmol/l potasu w przypadku:
- uczulenia na jedną z substancji czynnych lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6),
- niskiego stężenia potasu we krwi (hipokaliemii),
- wysokiego stężenia wodorowęglanu we krwi (alkalozy metabolicznej).
Nie można wykluczyć obecności antygenu kukurydzy w roztworze Prismasol.
Nie stosować hemofiltracji/dializy w następujących przypadkach:
- niewydolność nerek z wyraźnym hiperkatabolizmem (nieprawidłowy wzrost katabolizmu), jeśli objawów uremii (objawy spowodowane wysokim stężeniem mocznika we krwi) nie można
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
1/8
złagodzić za pomocą hemofiltracji;
- niewystarczające ciśnienie tętnicze w dostępie naczyniowym;
- antykoagulacja ogólnoustrojowa (zmniejszona krzepliwość krwi) przy zagrożeniu krwotokiem (krwawieniem).
Ostrzeżenia i środki ostrożności
Przed rozpoczęciem stosowania roztworu Prismasol należy zwrócić się do lekarza, farmaceuty lub
pielęgniarki.
Roztwór powinien być używany wyłącznie przez lub pod nadzorem lekarza wykwalifikowanego
w leczeniu niewydolności nerek przez zastosowanie hemofiltracji, hemodiafiltracji i ciągłej
hemodializy.
Przed zastosowaniem leczenia i podczas jego trwania zostanie zbadana krew pacjenta, np. będzie
monitorowana równowaga kwasowo-zasadowa i stężenie elektrolitów (soli we krwi), w tym również
wszelkich podawanych płynów (infuzje dożylne) oraz tworzonych przez organizm (wytwarzanie
moczu), nawet niezwiązanych bezpośrednio z terapią.
Należy dokładnie monitorować stężenie glukozy we krwi, zwłaszcza gdy pacjent choruje na cukrzycę.
Lek Prismasol a inne leki
Należy powiedzieć lekarzowi lub farmaceucie o wszystkich lekach przyjmowanych przez pacjenta
obecnie lub ostatnio a także o lekach, które pacjent planuje przyjmować.
Stężenie we krwi innych przyjmowanych leków może zostać obniżone podczas leczenia. Lekarz
zdecyduje, czy wymagana jest zmiana przyjmowanych leków.
W szczególności należy powiedzieć lekarzowi o przyjmowaniu następujących leków:
- glikozydów (stosowanych w leczeniu określonych chorób serca), gdyż podczas hipokaliemii (obniżonego stężenia potasu we krwi) zwiększają one ryzyko wystąpienia zaburzeń rytmu serca (nieregularnego lub przyspieszonego bicia serca);
- witaminy D i leków zawierających wapń, gdyż mogą one zwiększać ryzyko wystąpienia hiperkalcemii (wysokiego stężenia wapnia we krwi);
- jakichkolwiek dodatków sodu wodorowęglanu (lub innych buforów), gdyż może on zwiększać ryzyko wystąpienia zasadowicy metabolicznej (nadmiaru wodorowęglanów we krwi);
- cytrynianu, używanego jako środek hamujący krzepnięcie krwi (jako ochronny dodatek w sprzęcie do dializy), ponieważ może on zmniejszyć stężenie wapnia w osoczu.
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Lekarz zadecyduje o podawaniu roztworu Prismasol kobietom w ciąży lub karmiącym piersią.
Prowadzenie pojazdów i obsługiwanie maszyn
Nie wiadomo, czy Prismasol wpływa na zdolność prowadzenia pojazdów i obsługiwania maszyn.
3. Jak stosować Prismasol
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości
należy zwrócić się do lekarza lub farmaceuty.
Objętość używanego roztworu Prismasol zależy od stanu klinicznego pacjenta i docelowego bilansu
płynów. Dlatego decyzję o objętości dawki podejmuje lekarz odpowiedzialny za leczenie.
Droga podawania: do podawania dożylnego i hemodializy.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
2/8
Zastosowanie większej niż zalecana dawki leku Prismasol
Pacjent będzie miał dokładnie monitorowany bilans płynów, równowagę elektrolitową i kwasowo-
zasadową.
W mało prawdopodobnym przypadku wystąpienia przedawkowania lekarz podejmie niezbędne środki
zaradcze i dostosuje dawkę pacjenta.
Przedawkowanie może prowadzić do wystąpienia:
- przeciążenia płynami we krwi pacjenta,
- wzrostu stężenia wodorowęglanów we krwi (alkaloza metaboliczna)
- i (lub) zmniejszenia stężenia soli we krwi (hipofosfatemia, hipokaliemia). Przedawkowanie może prowadzić do poważnych następstw, takich jak zastoinowa niewydolność serca, zaburzenia równowagi elektrolitowej czy kwasowo-zasadowej.
Instrukcje użycia znajdują się w części „Informacje przeznaczone wyłącznie dla fachowego personelu
medycznego”.
W razie jakichkolwiek dalszych wątpliwości związanych ze stosowaniem tego leku, należy zwrócić
się do lekarza, farmaceuty lub pielęgniarki.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Zgłaszano następujące działania niepożądane:
Częstość nieznana: częstość nie może być określona na podstawie dostępnych danych
- zmiany stężenia soli we krwi (zaburzenia równowagi elektrolitowej, jak hipofosfatemia lub hipokaliemia)
- wzrost stężenia wodorowęglanów w osoczu (alkaloza metaboliczna) lub obniżenie stężenia wodorowęglanów w osoczu (kwasica metaboliczna)
- nieprawidłowo wysoka lub niska objętość wody w organizmie (hiper- lub hipowolemia)
- nieprawidłowo wysokie stężenie glukozy we krwi (hiperglikemia)
- nudności
- wymioty
- skurcze mięśni
- niedociśnienie (niskie ciśnienie krwi).
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione
w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce.
Działania
niepożądane
można
zgłaszać
bezpośrednio
do
Departamentu
Monitorowania
Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych,
Wyrobów Medycznych i Produktów Biobójczych
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301
Faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
3/8
5. Jak przechowywać Prismasol
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie przechowywać w temperaturze poniżej +4°C.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i opakowaniu. Termin
ważności oznacza ostatni dzień podanego miesiąca.
Wykazano chemiczną i fizyczną stabilność gotowego do użycia roztworu w ciągu 24 godzin w
temperaturze +22°C. Jeśli nie zostanie zużyty od razu, za czas i warunki przechowywania przed
zastosowaniem odpowiada użytkownik i czas ten nie powinien być dłuższy niż 24 godziny, włączając
czas leczenia.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera Prismasol
Substancje czynne:
Przed odtworzeniem/zmieszaniem:
1000 ml roztworu elektrolitowego (mała komora A) zawiera:
Wapnia chlorek dwuwodny
5,145 g
Magnezu chlorek sześciowodny
2,033 g
Glukoza
22,000 g
Kwas (S)-mlekowy
5,400 g
1000 ml roztworu buforowego (duża komora B) zawiera:
Sodu chlorek
6,450 g
Sodu wodorowęglan
3,090 g
Potasu chlorek
0,157 g
Po odtworzeniu/zmieszaniu:
Roztwory w komorach A (250 ml) i B (4750 ml) są mieszane w celu otrzymania jednego gotowego do
użycia roztworu (5000 ml) składającego się z:
mmol/l
mEq/l
Wapń
Ca
1,75
3,50
Magnez
Mg
0,50
1,00
Sód
Na
140,00
140,00
Chlorki
Cl
111,50
111,50
Mleczan
3,00
3,00
Wodorowęglan
HCO
32,00
32,00
Potas
K
2,00
2,00
Glukoza
6,10
Teoretyczna osmolarność:
297 mOsm/l
Pozostałe składniki leku to:dwutlenek węgla (E 290),woda do wstrzykiwań.
pH gotowego do użycia roztworu wynosi: 7,0 do 8,5
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
4/8
Jak wygląda Prismasol i co zawiera opakowanie
Prismasol jest pakowany w dwukomorowe worki zawierające w mniejszej komorze A roztwór
elektrolitowy, a w większej komorze B – roztwór buforowy. Ostateczny gotowy do użycia roztwór
uzyskuje się po złamaniu łamliwej zatyczki i wymieszaniu obu roztworów. Gotowy do użycia roztwór
jest przezroczysty i lekko żółty. Każdy worek (A+B) zawiera 5000 ml roztworu do hemofiltracji
i hemodializy. Worek jest umieszczony w przezroczystym opakowaniu zewnętrznym.
W każdym opakowaniu znajdują się dwa worki i ulotka informacyjna.
Podmiot odpowiedzialny i wytwórca:
Vantive Belgium SRL
Boulevard d’Angleterre 2
1420 Braine-l’Alleud
Belgia
Wytwórca:
Bieffe Medital S.p.A.,
Via Stelvio 94,
23035 Sondalo (SO),
Włochy
lub
Vantive Manufacturing Limited,
Moneen Road,
Castlebar
County Mayo
F23 XR63
Irlandia
Ten lek jest dopuszczony do obrotu w krajach członkowskich Europejskiego Obszaru
Gospodarczego i w Wielkiej Brytanii (Irlandii Pólnocnej) pod następującymi nazwami:
Austria, Belgia, Bułgaria, Cypr, Czechy, Dania, Estonia, Finlandia, Francja, Niemcy, Grecja, Węgry,
Islandia, Irlandia, Włochy, Łotwa, Litwa, Luksemburg, Malta, Holandia, Norwegia, Polska,
Portugalia, Rumunia, Słowacja, Słowenia, Hiszpania, Szwecja, Wielka Brytania (Irlandia Północna):
Prismasol 2.
Data ostatniej aktualizacji ulotki: wrzesień 2024
--------------------------------------------------------------------------------------------------------------------------
Informacje przeznaczone wyłącznie dla fachowego personelu medycznego:
Prismasol 2 mmol/l potasu roztwór do hemodializy/hemofiltracji
Środki ostrożności:
Należy ściśle przestrzegać instrukcji użycia/postępowania z produktem leczniczym Prismasol.
Roztwory z obu komór muszą zostać zmieszaneprzed użyciem.
Zastosowanie zanieczyszczonego roztworu do hemofiltracji oraz hemodializy może spowodować
sepsę, wstrząs lub stan zagrażający życiu.
Aby zwiększyć komfort pacjenta, produkt leczniczy Prismasol można ogrzać do temperatury 37°C.
Ogrzanie roztworu przed użyciem należy wykonać przed rekonstytucją i wyłącznie przy użyciu
suchego źródła ciepła. Roztworów nie należy ogrzewać w wodzie ani kuchence mikrofalowej. Przed
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
5/8
podaniem należy sprawdzić wizualnie roztwór w celu wykrycia obecności cząstek stałych oraz zmiany
zabarwienia, o ile roztwór oraz opakowanie na to pozwalają. Nie podawać roztworu, który nie jest
przezroczysty lub spaw został naruszony.
Roztwór ten zawiera potas. Stężenie potasu w surowicy musi być monitorowane przed zabiegiem
hemofiltracji i (lub) hemodializy oraz podczas jego trwania. Zależnie od stężenia potasu w surowicy
przed leczeniem może rozwinąć się hipokaliemia lub hiperkaliemia.
Jeśli wystąpi hipokaliemia, może być koniecznie dodanie potasu i (lub) podanie dializatu o wyższym
stężeniu potasu.
Jeśli po rozpoczęciu leczenia wystąpi hiperkaliemia, należy ocenić dodatkowe źródła wpływające na
stężenie potasu we krwi. Jeśli roztwór stosuje się jako roztwór substytucyjny, należy zmniejszyć
szybkość infuzji i potwierdzić, że osiągnięto żądane stężenie potasu. Jeśli hiperkaliemia nie ustąpi,
należy natychmiast przerwać infuzję.
Jeśli hiperkaliemia rozwinie się w przypadku stosowania roztworu jako dializatu, może być konieczne
podanie dializatu niezawierającego potasu w celu zwiększenia szybkości usuwania potasu.
Należy regularnie mierzyć stężenie nieorganicznych fosforanów. W przypadku niskiego stężenia
fosforanów we krwi, nieorganiczne fosforany muszą być uzupełniane. Do roztworu można dodać
fosforany w ilości do 1,2 mmol/l. W przypadku dodawania potasu fosforanu całkowite stężenie potasu
nie powinno przekraczać 4 mEq/l (4 mmol/l).
Choć w związku ze stosowaniem produktu leczniczego Prismasol nie zgłaszano przypadków ciężkich
reakcji nadwrażliwości na kukurydzę, roztwory zawierające glukozę uzyskaną z hydrolizowanej
skrobi kukurydzianej nie powinny być stosowane u pacjentów ze stwierdzoną alergią na kukurydzę
lub produkty kukurydziane.
Należy natychmiast przerwać podawanie w przypadku wystąpienia jakichkolwiek przedmiotowych
lub podmiotowych objawów podejrzewanej reakcji nadwrażliwości. Należy zastosować odpowiednie
terapeutyczne środki zaradcze, zgodnie ze wskazaniem klinicznym.
Ponieważ roztwór zawiera glukozę oraz mleczan, może się rozwinąć hiperglikemia, zwłaszcza
u pacjentów chorych na cukrzycę. Należy regularnie monitorować stężenie glukozy we krwi. Jeśli
rozwinie się hiperglikemia, może być konieczne podanie roztworu substytucyjnego/dializatu
niezawierającego glukozy. Mogą być konieczne inne środki zaradcze w celu utrzymania pożądanej
wartości glikemii.
Produkt leczniczy Prismasol zawiera wodorowęglan (dwuwęglan) oraz mleczan (prekursor
wodorowęglanu), które mogą wpływać na równowagę kwasowo-zasadową pacjenta. Jeśli w trakcie
leczenia z użyciem roztworu wystąpi lub pogłębi się alkaloza metaboliczna, może zaistnieć potrzeba
zmniejszenia szybkości podawania lub wstrzymania podawania produktu leczniczego.
Przed rozpoczęciem leczenia oraz podczas jego trwania, należy ściśle monitorować stężenie
elektrolitów oraz równowagę kwasowo-zasadową.
W przypadku braku równowagi płynów należy uważnie monitorować stan kliniczny pacjenta i w razie
potrzeby korygować bilans płynów.
Sposób podawania:
Do podawania dożylnego i hemodializy. Prismasol używany jako roztwór substytucyjny jest
podawany do obwodu przed hemofiltrem (predylucja) lub za hemofiltrem (postdylucja).
Dawkowanie:
Objętość oraz szybkość podawania używanego roztworu Prismasol zależy od stężenia elektrolitów we
krwi, równowagi kwasowo-zasadowej oraz ogólnego stanu klinicznego pacjenta. Parametry
podawania (dawkę, szybkość infuzji, całkowitą objętość) produktu Prismasol powinien ustalać lekarz.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
6/8
Szybkości przepływu dla roztworu substytucyjnego w hemofiltracji i hemodiafiltracji wynoszą:
Dorośli:
500 do 3000 ml/godz.
Szybkości przepływu dla roztworu do dializy (dializat) w ciągłej hemodializie i ciągłej
hemodiafiltracji wynoszą:
Dorośli:
500 do 2500 ml/godz.
Najczęściej stosowane szybkości przepływu w przypadku dorosłych wynoszą około 2000 do
2500 ml/godz., co odpowiada dobowej objętości płynu wynoszącej około 48 do 60 l.
Dzieci i młodzież
Zakres szybkości przepływu roztworu substytucyjnego w hemofiltracji i hemodiafiltracji oraz
roztworu do dializy (dializatu) w ciągłej hemodializie wynosi:
dzieci (od noworodków po młodzież do 18 lat): 1000 do 2000 ml/godz./1,73 m .
Wymagane szybkości przepływu mogą wynosić do 4000 ml/godz./1,73 m , zwłaszcza u młodszych
dzieci (≤10 kg). Bezwzględna szybkość przepływu (w ml/godz.) u dzieci i młodzieży zazwyczaj nie
powinna przekraczać maksymalnej szybkości przepływu stosowanej u dorosłych.
Instrukcja postępowania:
Aby uzyskać gotowy do użycia roztwór, roztwór elektrolitowy (mała komora A) jest dodawany do
roztworu buforowego (duża komora B) poprzez złamanie łamliwej zatyczki bezpośrednio przed
użyciem.
Należy stosować wyłącznie z odpowiednim sprzętem do pozaustrojowej wymiany nerkowej.
Podczas postępowania i podawania produktu pacjentowi należy stosować technikę aseptyczną.
Użyć wyłącznie, gdy opakowanie ochronne nie jest uszkodzone, wszystkie spawy są nienaruszone,
łamliwa zatyczka nie jest złamana, a roztwór jest przezroczysty. Ścisnąć mocno worek, aby sprawdzić
jego szczelność. W przypadku stwierdzenia przecieku roztwór należy natychmiast wyrzucić, ponieważ
nie można już zapewnić jego jałowości.
Duża komora B wyposażona jest w port do wstrzykiwań, umożliwiający po rekonstytucji roztworu,
dodanie innych niezbędnych produktów leczniczych. Lekarz jest odpowiedzialny za określenie
zgodności dodatkowych produktów leczniczych z roztworem Prismasol poprzez sprawdzanie czy nie
nastąpiła zmiana koloru i (lub) wytrącenie się osadu, nierozpuszczalnych kompleksów lub kryształów.
Przed dodaniem produktu leczniczego należy sprawdzić, czy jest rozpuszczalny i stabilny w wodzie o
pH takim jak roztwór Prismasol (pH gotowego do użycia roztworu wynosi od 7,0 do 8,5). Dodatkowe
składniki mogą być niezgodne. Należy zapoznać się z instrukcją dotyczącą stosowania dodawanego
produktu leczniczego.
Usunąć płyn z portu do wstrzykiwań, przytrzymać worek do góry nogami, wstrzyknąć produkt
leczniczy przez port i starannie wymieszać. Roztwór należy podać niezwłocznie. Dodatkowe składniki
muszą zawsze być dodane i zmieszane przed podłączeniem worka z roztworem do obwodu
pozaustrojowego.
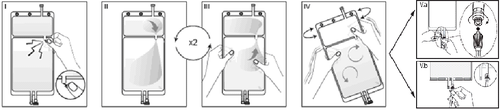
I
Opakowanie zewnętrzne zdjąć bezpośrednio przed użyciem i wyrzucić wszystkie pozostałe
materiały opakowaniowe. Otworzyć zamknięcie łamiąc łamliwą zatyczkę znajdującą się
pomiędzy dwiema komorami worka. Łamliwa zatyczka pozostanie w worku. (Patrz rysunek I
poniżej)
II
Upewnić się, że cały płyn z małej komory A został przelany do dużej komory B. (Patrz rysunek
II poniżej)
III
Przepłukać dwukrotniemałą komorę A, wyciskając zmieszany roztwór z powrotem do małej
komory A, a następnie ponownie do dużej komory B. (Patrz rysunek III poniżej)
IV
Gdy mała komora A jest pusta: potrząsać dużą komorą B w celu całkowitego wymieszania się
jej zawartości. Roztwór jest teraz gotowy do użycia i worek można zawiesić na stojaku. (Patrz
rysunek IV poniżej)
V
Do każdego z dwóch portów dostępu można podłączyć linię dializy lub wymiany.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
7/8
V.a
Jeśli korzysta się z dostępu typu luer, usunąć zatyczkę, przekręcając ją i pociągając, a następnie
podłączyć męską końcówkę luer lock linii dializy lub wymiany do żeńskiej końcówki typu luer
receptor na worku, dociskając ją i przekręcając. Upewnić się, że połączenie jest całkowicie
osadzone i pewne. Teraz złącze jest otwarte. Sprawdzić, czy płyn przepływa swobodnie. (Patrz
rysunek V.a poniżej)
Gdy linie dializy lub wymiany będą odłączone od złącza typu luer, połączenie zostanie
zamknięte i przepływ płynu wstrzymany. Port typu luer jest bezigłowy i można go przecierać
środkami dezynfekującymi.
V.bJeśli używany jest port do wstrzykiwań, najpierw usunąć zatyczkę poprzez jej odłamanie. Port
do wstrzykiwań można przecierać środkami dezynfekującymi. Następnie przebić kolcem
gumową przegrodę. Sprawdzić, czy płyn przepływa swobodnie. (Patrz rysunek V.b poniżej)
Roztwór należy użyć niezwłocznie po usunięciu zewnętrznego opakowania. Jeśli nie zostanie użyty od
razu, odtworzony roztwór należy użyć w ciągu 24 godzin, włączając w to czas zabiegu po dodaniu
roztworu elektrolitowego oraz roztworu buforowego.
Gotowy do użycia roztwór przeznaczony jest wyłącznie do jednorazowego użytku. Wyrzucić cały
niezużyty roztwór bezpośrednio po użyciu.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie
z lokalnymi przepisami.
Prismasol 2 mmol/l Potassium / PL / PL PVC luer connector with valve
8/8
- Страна регистрации
- Форма выпускаРаствор, 2 ммоль/л
- Отпускается по рецептуНет
- ИмпортерBieffe Medital S.p.A. Vantive Manufacturing Limited
- Информация на этой странице носит справочный характер и не является медицинской консультацией. Перед началом приема лекарства обязательно проконсультируйтесь с врачом.
- Аналоги ПрисмасолФорма выпуска: Раствор, 9 мг/млДействующее вещество: Хлорид натрияОтпускается по рецептуФорма выпуска: Раствор, 100 мг/млДействующее вещество: декстранаПроизводитель: Fresenius Kabi Italia S.r.L.Отпускается без рецептаФорма выпуска: Концентрат, -Действующее вещество: electrolytes in combination with other drugsПроизводитель: Fresenius Kabi Norge ASОтпускается без рецепта
Аналоги Присмасол в других странах
Лекарства с тем же действующим веществом, доступные в других странах.
Аналог Присмасол в Украина
Врачи онлайн по Присмасол
Обсудите применение Присмасол и возможные следующие шаги — по оценке врача.
Часто задаваемые вопросы

Получайте обновления и полезные материалы
Новости о медицинских услугах, обновления сервиса и практическая информация для пациентов.