Верораб

Інструкція із застосування Верораб
Перекладено з використанням ШІ
Інформація на цій сторінці має довідковий характер і не замінює консультацію лікаря. Перед застосуванням будь-яких лікарських засобів проконсультуйтеся з медичним фахівцем.
Показати перекладЗміст інструкції
- Ulotka dołączona do opakowania: informacja dla użytkownika
- Co to jest szczepionka VERORAB i w jakim celu się ją stosuje
- Informacje ważne przed zastosowaniem szczepionki VERORAB
- Kiedy nie stosować szczepionki VERORAB:
- Szczepienie przed ekspozycją
- Szczepienie po ekspozycji
- Ostrzeżenia i środki ostrożności
- Szczepionka VERORAB zawiera fenyloalaninę, potas i sód
- Szczepionka VERORAB a inne leki
- Ciąża, karmienie piersią i płodność
- Ciąża
- Karmienie piersią
- Płodność
- Prowadzenie pojazdów i obsługiwanie maszyn
- Jak stosować szczepionkę VERORAB
- Dawkowanie
- Tabela 1: Schemat szczepienia przed ekspozycją
- Dzień 0 Dzień 7 Dzień 21 lub 28
- Tabela 2: Kategorie ciężkości narażenia (ekspozycji) według WHO
- Tabela 3: Postępowanie w zależności od stanu zwierzęcia
- Stosowanie u osób z obniżoną odpornością
- Dzieci i młodzież
- Sposób podawania
- Zastosowanie większej niż zalecana dawki szczepionki VERORAB
- Pominięcie 1 dawki szczepionki VERORAB
- Przerwanie stosowania szczepionki VERORAB
- Możliwe działania niepożądane
- Jak przechowywać szczepionkę VERORAB
- Zawartość opakowania i inne informacje
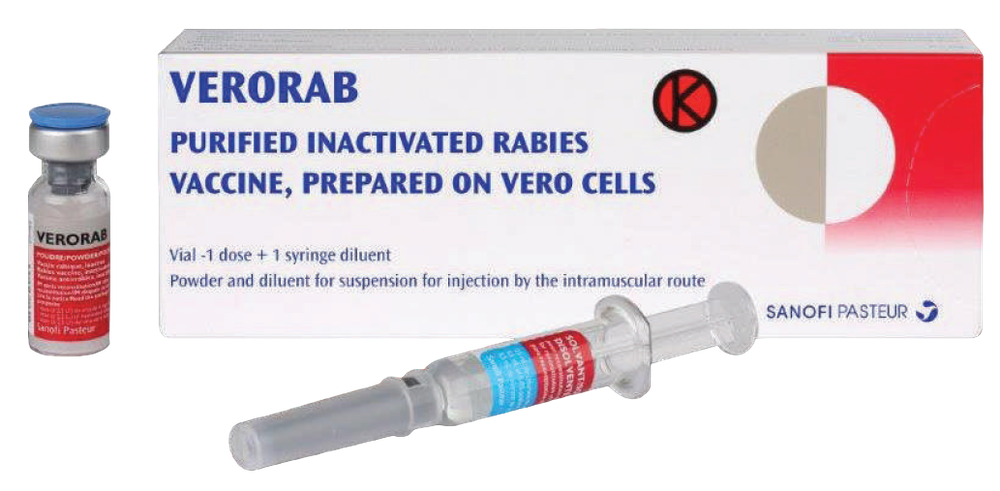
Ulotka dołączona do opakowania: informacja dla użytkownika
VERORAB,proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań
Szczepionka przeciw wściekliźnie stosowana u ludzi, produkowana w hodowlach komórkowych
Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem szczepionki, ponieważ zawiera ona informacje ważne dla pacjenta.
- Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać.
- W razie jakichkolwiek wątpliwości należy zwrócić się do lekarza lub farmaceuty.
- Szczepionkę tę przepisano ściśle określonej osobie. Nie należy jej przekazywać innym. Szczepionka ta może zaszkodzić innej osobie.
- Jeśli u pacjenta wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie objawy niepożądane niewymienione w tej ulotce, należy powiedzieć o tym lekarzowi. Patrz punkt 4.
Spis treści ulotki
- 1. Co to jest szczepionka VERORAB i w jakim celu się ją stosuje
- 2. Informacje ważne przed zastosowaniem szczepionki VERORAB
- 3. Jak stosować szczepionkę VERORAB
- 4. Możliwe działania niepożądane
- 5. Jak przechowywać szczepionkę VERORAB
- 6. Zawartość opakowania i inne informacje
1. Co to jest szczepionka VERORAB i w jakim celu się ją stosuje
Szczepionka VERORAB jest wskazana do zapobiegania wściekliźnie przed i po kontakcie z wirusem
wścieklizny we wszystkich grupach wiekowych.
Zapobieganie wściekliźnie przed ekspozycją (szczepienie przed ekspozycją)
Szczepienie przed ekspozycją powinno być proponowane osobom z grup wysokiego ryzyka zakażenia
się wirusem wścieklizny.
Powinni być szczepieni wszyscy, którzy są stale narażeni na zakażenie np. pracownicy laboratoriów
z działu diagnostycznego, naukowo-badawczego i produkcyjnego wykonujący prace z wirusem
wścieklizny. Odporność powinna być podtrzymywana poprzez stosowanie dawek przypominających
(patrz „Dawkowanie”).
Szczepienie jest także zalecane dla poniżej wymienionych grup, biorąc pod uwagę częstość narażenia
na ryzyko zakażenia:
- lekarze weterynarii i ich asystenci, opiekunowie zwierząt (łącznie z tymi, którzy mają kontakt z nietoperzami) oraz leśnicy (myśliwi) i preparatorzy zwierząt,
- osoby, mające kontakt z potencjalnie wściekłymi zwierzętami (takimi jak psy, koty, skunksy, szopy pracze, nietoperze),
- dorośli i dzieci przebywające lub podróżujące do obszarów, gdzie występuje zagrożenie zakażenia się wścieklizną.
2. Informacje ważne przed zastosowaniem szczepionki VERORAB
Kiedy nie stosować szczepionki VERORAB:
Szczepienie przed ekspozycją
- jeśli pacjent ma uczulenie na szczepionkę lub którykolwiek z pozostałych składników tej szczepionki (wymienionych w punkcie 6.),
- jeśli wystąpiła reakcja alergiczna po poprzednim podaniu szczepionki VERORAB lub jakiejkolwiek innej szczepionki o takim samym składzie,
- jeśli występuje gorączka lub ostra choroba (w tym przypadku preferowane jest przełożenie szczepienia).
Szczepienie po ekspozycji
- Biorąc pod uwagę fakt, że potwierdzone zakażenie wścieklizną jest śmiertelne, nie istnieją żadne przeciwwskazania do szczepienia po ekspozycji.
Ostrzeżenia i środki ostrożności
- Tak jak w przypadku wszystkich szczepionek, VERORAB może nie chronić 100% zaszczepionych osób.
- Szczepionki VERORAB nie wolno podawać donaczyniowo; należy upewnić się, że igła nie tkwi w naczyniu krwionośnym.
- Należy stosować ostrożnie u osób z alergią na polimyksynę B, streptomycynę, neomycynę (są obecne w szczepionce w ilościach śladowych) lub inny antybiotyk z tej samej grupy.
- Jeśli szczepionka podawana jest osobom ze znanym obniżeniem odporności z powodu choroby lub leczenia, w okresie 2 do 4 tygodni po szczepieniu należy wykonać badanie serologiczne, patrz „Dawkowanie”.
- Szczepionka VERORAB powinna być podawana ostrożnie osobom z obniżoną liczbą płytek krwi (trombocytopenia) lub zaburzeniami krzepnięcia z uwagi na ryzyko krwawienia, które może wystąpić po wstrzyknięciu domięśniowym.
Szczepionka VERORAB zawiera fenyloalaninę, potas i sód
- Szczepionka VERORAB zawiera 4,1 mikrogramów fenyloalaniny w każdej dawce 0,5 ml, co odpowiada 0,068 mikrograma/kg dla osoby o masie 60 kg. Fenyloalanina może być szkodliwa w przypadku pacjentów chorych na fenyloketonurię, rzadką chorobę genetyczną, w której fenyloalanina gromadzi się, ponieważ organizm nie może jej usunąć we właściwy sposób.
- Szczepionka VERORAB zawiera mniej niż 1 mmol potasu (39 mg) i sodu (23 mg) na dawkę, to znaczy szczepionkę uznaje się za „wolną od potasu” i „wolną od sodu”.
Szczepionka VERORAB a inne leki
Leki immunosupresyjne, w tym długotrwała terapia ogólnoustrojowymi kortykosteroidami, mogą
wpłynąć niekorzystnie na wytwarzanie przeciwciał i spowodować, że szczepienie będzie nieskuteczne.
Dlatego wskazane jest wykonanie badania serologicznego 2 do 4 tygodni po ostatnim szczepieniu,
patrz „Ostrzeżenia i środki ostrożności”.
Dorośli i dzieci mogą otrzymać szczepionkę VERORAB w tym samym czasie, co szczepionkę
przeciw durowi brzusznemu. Szczepionki te muszą być podawane w różne części ciała i nie mogą być
mieszane w tej samej strzykawce.
W przypadku jednoczesnego podawania z jakimkolwiek innym produktem leczniczym, w tym z
immunoglobulinami przeciw wściekliźnie, szczepienie należy wykonać w różne miejsca oraz użyć
oddzielnych strzykawek.
Ponieważ immunoglobulina przeciw wściekliźnie wpływa na rozwój odpowiedzi immunologicznej na
szczepionkę, należy ściśle przestrzegać zaleceń dotyczących podawania immunoglobuliny przeciw
wściekliźnie.
Należy powiedzieć lekarzowi o wszystkich lekach przyjmowanych przez pacjenta obecnie lub
ostatnio, a także o lekach, które pacjent planuje przyjmować.
Ciąża, karmienie piersią i płodność
Ciąża
Jedno badanie toksyczności u zwierząt przeprowadzone z inną inaktywowaną szczepionką przeciw
wściekliźnie VERORABVAX nie wykazało szkodliwego wpływu na płodność samic ani na rozwój
płodu.
Kliniczne zastosowanie szczepionek przeciw wściekliźnie (inaktywowany szczep „WISTAR Rabies
PM/WI38 1503-3M”) u niewielkiej liczby kobiet w ciąży nie wykazało zniekształcającego ani
toksycznego działania na płód.
Biorąc pod uwagę ciężki przebieg choroby, w przypadku wysokiego ryzyka zakażenia szczepienie
w okresie ciąży, powinno być przeprowadzone zgodnie z zalecanym schematem szczepienia.
Karmienie piersią
Ta szczepionka może być stosowana w okresie karmienia piersią.
Jeśli pacjentka jest w ciąży lub karmi piersią, przypuszcza że może być w ciąży lub gdy planuje mieć
dziecko, powinna poradzić się lekarza przed zastosowaniem tej szczepionki.
Płodność
Szczepionka nie była oceniana pod kątem zaburzania płodności u mężczyzn lub kobiet.
Prowadzenie pojazdów i obsługiwanie maszyn
Po szczepieniu, często zgłaszano zawroty głowy co może przejściowo wpływać na zdolność
prowadzenia pojazdów i obsługiwanie maszyn.
3. Jak stosować szczepionkę VERORAB
Tę szczepionkę należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości należy
zwrócić się do lekarza lub farmaceuty.
Dawkowanie
Do podania domięśniowego ( im.) zalecana dawka to 0,5 ml szczepionki po rekonstytucji.
Do podania śródskórnego ( id.) zalecana dawka to 0,1 ml szczepionki po rekonstytucji w każde miejsce
podania.
VERORAB może być podawany u dzieci i dorosłych w tych samych dawkach.
Profilaktyka przed ekspozycją
W ramach szczepienia przed ekspozycją, pacjenci mogą otrzymać szczepionkę według jednego ze
schematów szczepienia przedstawionych w Tabeli 1 oraz zgodnie z oficjalnymi lokalnymi
zaleceniami, jeżeli są dostępne.
Tabela 1: Schemat szczepienia przed ekspozycją
Dzień 0 Dzień 7 Dzień 21 lub 28
Podanie domięśniowe (dawka 0,5 ml)
Schemat tradycyjny
Podanie im. – 0,5 ml
1 dawka
1 dawka
1 dawka
Schemat tygodniowy
Podanie im. – 0,5 ml
1 dawka
1 dawka
Podanie śródskórne (dawka 0,1 ml)
Schemat tygodniowy
Podanie id. – 0,1 ml
2 dawki
2 dawki
Profilaktyka po ekspozycji
Profilaktykę po ekspozycji należy rozpocząć jak najszybciej po podejrzewanym kontakcie z wirusem
wścieklizny.
We wszystkich przypadkach należy natychmiast, lub jak najszybciej po ekspozycji, odpowiednio
opatrzyć ranę (dokładnie przepłukać i przemyć mydłem lub detergentem oraz dużą ilością wody i (lub)
środków wirusobójczych wszystkie rany po ugryzieniu i zadrapania). Należy to zrobić przed
podaniem szczepionki przeciw wściekliźnie lub immunoglobuliny przeciw wściekliźnie, jeśli są one
wskazane.
Szczepionkę przeciw wściekliźnie należy podawać ściśle według stopnia narażenia (kategorii
ekspozycji), stanu uodpornienia pacjenta i stanu zwierzęcia pod kątem wścieklizny (zgodnie z
oficjalnymi lokalnymi zaleceniami, patrz Tabela 2 z zaleceniami WHO).
Szczepienie po ekspozycji musi być przeprowadzane pod nadzorem lekarza, w specjalistycznym
ośrodku i jak najszybciej po ekspozycji.
Jeśli jest to konieczne, leczenie może być uzupełnione o profilaktykę przeciwtężcową
i antybiotykoterapię, żeby zapobiec zakażeniu innemu niż wścieklizna.
Tabela 2: Kategorie ciężkości narażenia (ekspozycji) według WHO
| Kategoria narażenia (ekspozycji) | Rodzaj kontaktu z domowym lub dzikim zwierzęciem podejrzanym o wściekliznę lub z potwierdzoną wścieklizną lub zwierzęciem niedostępnym do badania | Zalecana profilaktyka po ekspozycji |
| I | Dotknięcie lub karmienie zwierząt. Oślinienie skóry o nienaruszonej ciągłości. (brak narażenia) | Nie ma, jeśli jest dostępna wiarygodna dokumentacja medycznaa. |
| II | Niewielkie ugryzienia odsłoniętej skóry. Niewielkie zadrapania lub otarcia bez krwawienia. (narażenie) | Natychmiast podać szczepionkę. Przerwać leczenie, jeśli w ciągu 10-dniowej obserwacji zwierzę pozostaje zdroweb lub jeśli u zwierzęcia potwierdzono negatywny wynik badania na obecność wirusa wścieklizny przeprowadzonego przez wiarygodne laboratorium, przy użyciu odpowiednich technik diagnostycznych. Kontakt z nietoperzem należy traktować jako kategorię III. |
| III | Pojedyncze albo mnogie ugryzienia luz zadrapania przechodzące przez całą grubość skóryc, oślinienie błon śluzowych lub uszkodzonej skóry śliną zwierząt, narażenie w wyniku bezpośredniego kontaktu z nietoperzami. (ciężkie narażenie) | Natychmiast podać szczepionkę przeciw wściekliźnie i immunoglobulinę, najlepiej jak najszybciej po rozpoczęciu profilaktyki po ekspozycji. Immunoglobulina przeciw wściekliźnie może być podana do 7 dni po podaniu pierwszej dawki szczepionki. Przerwać leczenie, jeśli w ciągu 10-dniowej obserwacji zwierzę pozostaje zdrowe lub jeśli u zwierzęcia potwierdzono negatywny wynik badania na obecność wirusa wścieklizny przeprowadzonego przez wiarygodne laboratorium, przy użyciu odpowiednich technik diagnostycznych. |
a Jeżeli pies lub kot pochodzący z rejonu o niskim ryzyku zakażenia lub przebywający na takim
obszarze nie ma objawów choroby i jest poddany obserwacji, leczenie może być odłożone.
b Ten okres obserwacji dotyczy tylko psów i kotów. Z wyjątkiem gatunków zagrożonych, inne
domowe lub dzikie zwierzęta podejrzane o wściekliznę powinny być poddane eutanazji, a ich
tkanki zbadane pod kątem obecności antygenu wścieklizny przy użyciu odpowiednich technik
laboratoryjnych.
c Ugryzienia, w szczególności okolic głowy, szyi, twarzy, dłoni i genitaliów są klasyfikowane jako
kategoria III z powodu silnego unerwienia tych miejsc.
Tabela 3: Postępowanie w zależności od stanu zwierzęcia
| Okoliczności | Postępowanie dotyczące | Uwagi | |
| zwierząt | pacjenta | ||
| Zwierzę jest niedostępne Okoliczności podejrzane lub niestwarzające podejrzeń. | Przewóz do specjalistycznego ośrodka leczenia wścieklizny w celu leczenia. | Leczenie(b) jest zawsze pełne. | |
| Zwierzę nie żyje Okoliczności podejrzane lub niestwarzające podejrzeń. | Przesłać mózg do badania do uprawionego laboratorium. | Przewóz do specjalistycznego ośrodka leczenia wścieklizny w celu leczenia. | Leczenie(b) jest przerwane, jeśli wynik badania jest ujemny lub w przeciwnym razie jest kontynuowane. |
| Zwierzę żyje Okoliczności niestwarzające podejrzeń. | Poddać obserwacji weterynaryjnej(a). | Odroczenie leczenia przeciw wściekliźnie. | Leczenie(b) jest zastosowane w zależności od wyniku obserwacji weterynaryjnej zwierzęcia. |
| Zwierzę żyje Podejrzane okoliczności. | Poddać obserwacji weterynaryjnej(a). | Przewóz do specjalistycznego ośrodka leczenia wścieklizny w celu leczenia. | Leczenie(b) jest przerwane, jeśli obserwacja weterynaryjna nie potwierdzi początkowych wątpliwości lub w przeciwnym razie jest kontynuowane. |
We Francji w ramach obserwacji weterynaryjnej wydaje się 3 świadectwa - w 0, 7 i 14
dniu obserwacji – świadczące o braku objawów wścieklizny.
Według zaleceń WHO, dla psów i kotów minimalny okres obserwacji weterynaryjnej wynosi 10 dni.
Leczenie jest zalecane w zależności od ciężkości rany: patrz Tabela 2
Profilaktyka po ekspozycji osób wcześniej nieszczepionych
- Schemat Essen - szczepionkę podaje się w 0., 3., 7, 14. i 28. dniu (w sumie 5 wstrzyknięć po 0,5 ml) lub
- Schemat Zagrzeb (schemat 2-1-1) W dniu 0. podawana jest jedna dawka szczepionki w prawy mięsień naramienny i jedna dawka w lewy mięsień naramienny, następnie w dniu 7. i 21. podawana jest jedna dawka w okolicę mięśnia naramiennego (w sumie 4 wstrzyknięcia po 0,5 ml). U małych dzieci szczepionka jest podawana w przednio-boczną część uda.
W przypadku III kategorii ekspozycji (patrz Tabela 2), immunoglobulina przeciw wściekliźnie
powinna być podawana jednocześnie ze szczepionką. W takim przypadku, jeśli to możliwe,
szczepionka powinna być podana w inne miejsce, po przeciwnej stronie ciała.
W celu uzyskania dalszych informacji patrz: Ulotka informacyjna dla zastosowanej immunoglobuliny.
Szczepienia nie należy przerywać, chyba że na podstawie oceny lekarza weterynarii (obserwacja
zwierzęcia i (lub) analiza laboratoryjna) stwierdzono, że zwierzę nie ma wścieklizny.
Profilaktyka po ekspozycji osób uprzednio zaszczepionych
Zgodnie z zaleceniami WHO, osoby uprzednio zaszczepione to pacjenci, którzy mogą
udokumentować pełną wcześniejszą profilaktykę przed ekspozycją (ang. pre-exposure prophylaxis,
PrEP) lub profilaktykę po ekspozycji (ang. post-exposure prophylaxis, PEP) oraz osoby, które
przerwały serię PEP po co najmniej dwóch dawkach szczepionki przeciw wściekliźnie namnożonej na
liniach komórkowych.
Osoby wcześniej zaszczepione powinny otrzymać po jednej dawce szczepionki domięśniowo w
dniach 0 i 3. Immunoglobulina przeciw wściekliźnie nie jest wskazana u tych osób.
Stosowanie u osób z obniżoną odpornością
- Profilaktyka przed ekspozycją U osób z obniżoną odpornością należy zastosować tradycyjny 3-dawkowy schemat szczepienia (przedstawiony w podpunkcie „profilaktyka przed ekspozycją”) oraz wykonać badanie serologiczne przeciwciał neutralizujących, od 2 do 4 tygodni po ostatniej dawce, aby potwierdzić ewentualną potrzebę podania dodatkowej dawki szczepionki.
- Profilaktyka po ekspozycji U osób z obniżoną odpornością, należy stosować tylko pełny schemat szczepienia (wymieniony w podpunkcie „Profilaktyka po ekspozycji u osób wcześniej nieszczepionych”). Immunoglobulina przeciw wściekliźnie powinna być podana w skojarzeniu ze szczepionką dla dwóch kategorii ekspozycji: II i III (patrz Tabela 2).
Dzieci i młodzież
U dzieci i młodzieży należy stosować taką samą dawkę jak u dorosłych (0,5 ml domięśniowo lub
0,1 ml śródskórnie).
Sposób podawania
- Podanie domięśniowe ( im.) Szczepionkę podaje się w przednio-boczną część mięśnia uda u niemowląt i małych dzieci oraz w mięsień naramienny u starszych dzieci i dorosłych.
- Podanie śródskórne ( id.) Szczepionkę najlepiej podawać w górną część ramienia lub w przedramię.
Jeśli stosowane jest szczepienie według schematu Zagrzeb, w dniu 0 jedna dawka powinna być
podana w każdy mięsień naramienny (lewy i prawy) a następnie jedna dawka w dniu 7 i dniu 21.
Szczepionki VERORAB nie wolno podawać w okolicę mięśni pośladkowych.
Szczepionki nie wolno podawać donaczyniowo.
Zastosowanie większej niż zalecana dawki szczepionki VERORAB
Nie ma zastosowania.
Pominięcie 1 dawki szczepionki VERORAB
Lekarz zadecyduje kiedy podać pominiętą dawkę.
Przerwanie stosowania szczepionki VERORAB
Nie ma zastosowania.
4. Możliwe działania niepożądane
Jak każdy lek, lek ten może powodować działania niepożądane chociaż nie u każdego one wystąpią.
Ciężkie reakcje alergiczne:
Ciężkie reakcje alergiczne (reakcje anafilaktyczne) mogą wystąpić zawsze, nawet jeśli są bardzo
rzadkie. Jeśli u pacjenta lub u dziecka wystąpi reakcja anafilaktyczna, należy natychmiast
skontaktować się z lekarzem lub pracownikiem fachowego personelu medycznego lub natychmiast
udać się do najbliższego szpitalnego oddziału ratunkowego.
Objawy reakcji anafilaktycznej pojawiają się zazwyczaj bardzo szybko po wstrzyknięciu i mogą
obejmować wysypkę, swędzenie, trudności w oddychaniu, duszność, obrzęk twarzy, ust, gardła lub
języka.
Inne działania niepożądane:
Większość działań niepożądanych pojawia się w ciągu 3 dni po szczepieniu i ustępuje samoistnie w
ciągu 1 do 3 dni po ich wystąpieniu. Były one zgłaszane z następującą częstością:
Bardzo często: mogą wystąpić u więcej niż 1 na 10 osób
- Ogólne złe samopoczucie
- Ból głowy
- Ból mięśni
- Ból w miejscu wstrzyknięcia
- Zaczerwienienie w miejscu wstrzyknięcia
- Opuchnięcie w miejscu wstrzyknięcia
- Tylko u niemowląt - drażliwość, nieutulony płacz, senność
Często: mogą wystąpić u maksymalnie 1 na 10 osób
- Gorączka
- Powiększenie węzłów chłonnych
- Reakcje alergiczne, takie jak wysypka i swędzenie
- Objawy grypopodobne
- Swędzenie w miejscu wstrzyknięcia
- Stwardnienie w miejscu wstrzyknięcia
- Tylko u niemowląt - trudności w zasypianiu
Niezbyt często: mogą wystąpić u maksymalnie 1 na 100 osób
- Zmniejszony apetyt
- Nudności
- Ból brzucha
- Biegunka
- Wymioty
- Dreszcze
- Zmęczenie, nietypowe osłabienie
- Zawroty głowy
- Ból stawów
- Zasinienie w miejscu wstrzyknięcia
Rzadko: mogą wystąpić u maksymalnie 1 na 1000 osób
- Trudności w oddychaniu
Częstość nieznana: częstość nie może być określona na podstawie dostępnych danych
- Obrzęk twarzy, warg, ust, języka lub gardła, który może powodować trudności w połykaniu lub oddychaniu
- Nagły niedosłuch czuciowo-nerwowy
Zgłaszanie działań niepożądanych
Jeśli wystąpią jakiekolwiek działania niepożądane, w tym wszelkie objawy niepożądane
niewymienione w ulotce, należy powiedzieć o tym lekarzowi, farmaceucie lub pielęgniarce. Działania
niepożądane można zgłaszać bezpośrednio do Departamentu Monitorowania Niepożądanych Działań
Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
i Produktów Biobójczych:
Al. Jerozolimskie 181C
02-222 Warszawa
Tel.: + 48 22 49 21 301; faks: + 48 22 49 21 309
Strona internetowa: https://smz.ezdrowie.gov.pl
Działania niepożądane można zgłaszać również podmiotowi odpowiedzialnemu.
Dzięki zgłaszaniu działań niepożądanych można będzie zgromadzić więcej informacji na temat
bezpieczeństwa stosowania leku.
5. Jak przechowywać szczepionkę VERORAB
Należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w lodówce (2 ° C – 8 ° C). Nie zamrażać.
Przechowywać w oryginalnym opakowaniu zewnętrznym, w celu ochrony przed światłem.
Nie stosować tej szczepionki po upływie terminu ważności zamieszczonego na opakowaniu po EXP.
Termin ważności (EXP) oznacza ostatni dzień podanego miesiąca.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać
farmaceutę, jak usunąć leki, których się już nie używa. Takie postępowanie pomoże chronić
środowisko.
6. Zawartość opakowania i inne informacje
Co zawiera szczepionka VERORAB
- Po rekonstytucji w 0,5 ml rozpuszczalnika, 1 fiolka zawiera: Wirus wścieklizny , szczep Wistar Rabies PM/WI38 1503-3M (inaktywowany) 3,25 j.m. namnażany w komórkach VERO ilość oznaczana za pomocą testu ELISA zgodnie z międzynarodowym standardem.
- Pozostałe składniki to: Proszek: maltoza, 20% roztwór albuminy ludzkiej, podłoże Basal Medium Eagle (mieszanina soli mineralnych, w tym potas, witamin, dekstrozy i aminokwasów w tym fenyloalanina), woda do wstrzykiwań, kwas solny, wodorotlenek sodu. Rozpuszczalnik: sodu chlorek, woda do wstrzykiwań.
Jak wygląda szczepionka VERORAB i co zawiera opakowanie
1 fiolka z proszkiem + 1 ampułko-strzykawka z igłą z rozpuszczalnikiem po 0,5 ml –
w tekturowym pudełku.
10 fiolek z proszkiem + 10 ampułko-strzykawek z igłą z rozpuszczalnikiem po 0,5 ml –
w tekturowym pudełku.
5 fiolek z proszkiem + 5 ampułek z rozpuszczalnikiem po 0,5 ml – w tekturowym pudełku.
Podmiot odpowiedzialny i wytwórca
Podmiot odpowiedzialny
Sanofi Winthrop Industrie
82 Avenue Raspail
94250 Gentilly, Francja
Wytwórca
Sanofi Winthrop Industrie
1541 avenue Marcel Mérieux
69280 Marcy l’Etoile, Francja
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d’Incarville
B.P 101
27100 Val de Reuil, Francja
Sanofi-Aventis Zrt.
Bdg. DC5 - Campona Utca 1.
Budapest XXII - 1225 Budapest - Węgry
Data ostatniej aktualizacji ulotki:grudzień 2024
Informacje przeznaczone wyłącznie dla personelu medycznego:
Zalecenia odnośnie schematu szczepienia powinny być skrupulatnie przestrzegane.
Ampułko-strzykawka
Instrukcja użycia:
- Usunąć uszczelnienie fiolki z liofilizowanym proszkiem.
- Wkręcić tłok do strzykawki, jeśli jest dostarczany osobno.
- Wstrzyknąć rozpuszczalnik do fiolki z liofilizowanym proszkiem.
- Delikatnie obracać fiolkę, aż do uzyskania jednorodnej zawiesiny.
- Szczepionka po rekonstytucji powinna być przejrzysta, jednorodna i pozbawiona cząstek.
- Wyrzucić strzykawkę użytą do rekonstytucji szczepionki.
- Użyć nowej strzykawki z nową igłą do pobrania przygotowanej szczepionki.
- Należy wymienić igłę użytą do pobrania przygotowanej szczepionki na nową igłę do wstrzyknięcia domięśniowego lub śródskórnego. Długość igły używanej do podania szczepionki powinna być dostosowana do pacjenta.
Ampułka
Instrukcja użycia:
- Usunąć uszczelnienie fiolki z liofilizowanym proszkiem.
- Odłamać górną część ampułki. Nabrać rozpuszczalnik za pomocą strzykawki.
- Wstrzyknąć rozpuszczalnik do fiolki z liofilizowanym proszkiem.
- Delikatnie obracać fiolkę, aż do uzyskania jednorodnej zawiesiny.
- Szczepionka po rekonstytucji powinna być przejrzysta, jednorodna i pozbawiona cząstek.
- Pobrać zawiesinę za pomocą strzykawki.
- Należy wymienić igłę użytą do pobrania przygotowanej szczepionki na nową igłę do wstrzyknięcia domięśniowego lub śródskórnego. Długość igły używanej do podania szczepionki powinna być dostosowana do pacjenta.
Jeśli szczepionka VERORAB jest podawana drogą domięśniową, musi być zużyta natychmiast po
rekonstytucji.
Jeśli szczepionka VERORAB jest podawana drogą śródskórną, szczepionkę można zużyć w ciągu 6
godzin po rekonstytucji pod warunkiem przechowywania w temperaturze do 25 ºC, chroniąc przed
światłem. Po rekonstytucji w 0,5 ml rozpuszczalnika, dawki 0,1 ml szczepionki należy pobrać z fiolki
zachowując warunki aseptyczne. Pozostałość może być użyta dla innego pacjenta. Przed każdym
pobraniem delikatnie obracać fiolkę, aż do uzyskania jednorodnej zawiesiny. Należy użyć nowej igły i
strzykawki do pobrania i podania każdej dawki szczepionki każdemu pacjentowi, by uniknąć
zakażenia krzyżowego. Niezużytą szczepionkę należy wyrzucić po 6 godzinach.
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć w sposób
zgodny z lokalnymi przepisami.
Ten produkt leczniczy jest wydawany na receptę.
- Країна реєстрації
- Лікарська формаПорошок, 3,25 МО вірусу сказу, штам Wistar Rabies PM/WI38 1503-3M (інактивований)/0,5 мл; 1 доза (0,5 мл)
- Код АТХJ07BG01
- Діюча речовина
- Потрібен рецептТак
- ІмпортерSanofi Winthrop Industrie Sanofi Winthrop Industrie Sanofi-Aventis Zrt.
- Ця інформація надана лише для ознайомлення і не є медичною порадою. Рішення щодо лікування завжди приймає лікар.
- Альтернативи до ВерорабЛікарська форма: Порошок, не менше 2,5 МО вірусу сказу, штам Flury LEP (інактивований); 1 доза (1 мл)Діюча речовина: rabies, inactivated, whole virusПотрібен рецептЛікарська форма: Суспензія, 160 антигенних одиниць ELISA вірусу гепатиту A, штам GBM/0,5 мл; 1 доза (0,5 мл)Діюча речовина: hepatitis A, inactivated, whole virusПотрібен рецептЛікарська форма: Суспензія, 60 мкг HA/штам, 1 доза (0,7 мл)Діюча речовина: influenza, inactivated, split virus or surface antigenПотрібен рецепт
Аналоги Верораб в інших країнах
Препарати з тією самою діючою речовиною, доступні в інших країнах.
Аналог Верораб у Україна
Лікарі онлайн щодо Верораб
Застосування, безпека та можливість призначення рецепта — за результатами медичної оцінки.
Отримайте рецепт на Верораб онлайн
Заповніть форму за 2 хвилини
Розкажіть про симптоми, історію хвороби та потрібний препарат.
Оберіть лікаря або ми призначимо
Оберіть спеціаліста або ми підберемо найближчого доступного лікаря.
Лікар розглядає ваш випадок
Зазвичай протягом 30 хвилин. Може ставити уточнювальні запитання в чаті.
Отримайте в будь-якій аптеці
Електронний рецепт надсилається на вашу пошту — дійсний по всій Іспанії.
Часті запитання

Будьте в курсі новин Oladoctor
Інформація про нові послуги, оновлення сервісу та корисні матеріали для пацієнтів.